Selektiv vasopressinantagonist.
Anvendelsesområder
Voksne med hyponatriæmi sekundært til Schwartz-Bartters syndrom (SIADH).
Dispenseringsform
Tabletter. 1 tablet indeholder 7,5 mg, 15 mg eller 30 mg tolvaptan.
Doseringsforslag
Voksne
- Initialt 15 mg dgl. Dosis kan øges med 24 timers mellemrum til maksimalt 60 mg dgl.
- Ved risiko for meget hurtig korrektion af natrium, fx onkologiske tilstande, meget lav baseline-værdi af serum-natrium eller samtidig indtag af diuretika eller natriumtilskud bør en dosis på 7,5 mg overvejes.
- Behandling bør indledes på et hospital pga. behov for nøje kontrol af serum-natrium og volumenstatus i titreringsfasen.
Bemærk:
- Væskerestriktion bør undgås de første 24 timer pga. risiko for uønsket hurtig stigning af serum-natrium.
- Erfaring savnes vedr. børn og unge < 18 år.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-18 årErfaring savnes ved behandling af børn og unge under 18 år. Sikkerhed og virkning er ikke klarlagt.
Håndtering
| tabletter 7,5 mg |
| tabletter 15 mg |
| tabletter 30 mg |
Knusning/åbning
Kan knuses.
Administration
Knust tablet kan opslæmmes i vand.
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på kold, blød mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
forsigtighed, monitorering |
|
|---|---|
| GFR | Advarsel |
| <60 ml/min. |
Væske- og elektrolytbalance skal kontrolleres jævnligt. Erfaring savnes ved GFR < 30 ml/min. |
Nedsat leverfunktion
Kontraindikationer
- Anuri
- Volumendepletering
- Hypovolæmisk hyponatriæmi
- Hypernatriæmi
- Manglende tørstfornemmelse.
Forsigtighedsregler
Forsigtighed ved
- Urinvejsobstruktion
- Diabetes, da tolvaptan kan forårsage hyperglykæmi.
- Kendt overfølsomhed over for mirtazapin pga. øget risiko for overfølsomhedsreaktioner med tolvaptan.
- Væske- og elektrolytbalance skal kontrolleres jævnligt hos alle patienter, især ved nedsat nyre- og leverfunktion.
Skærpet advarsel mod risiko for for hurtig forøgelse af serum-natrium.
- Kontrol af serum-natrium indledes senest 6 timer efter påbegyndt behandling, og serum-natrium og volumenstatus kontrolleres mindst hver 6. time de første 1-2 dage, og indtil dosis er stabiliseret.
- Serum-natrium bør monitoreres nøje ved patienter med serum-natrium < 120 mmol/l og ved høj risiko for demyelineringssyndrom, fx ved hypoxi, alkoholisme eller fejlernæring.
- Natriumkorrektion, der overstiger 6 mmol/l i de første 6 timer eller 8 mmol/l under de første 6-12 timer, kan være for hurtig. Nøje monitorering af serum-natrium og administration af hypotonisk væske anbefales.
- Hvis forhøjelsen i serum-natrium er for hurtig (dvs. den overstiger 12 mmol/l på 24 timer eller 18 mmol/l på 48 timer), bør behandling seponeres eller ophøre og efterfølges af administration af hypotonisk væske.
- Samtidig administration af tolvaptan og medicin med et højt natriumindhold eller andre behandlinger af hyponatriæmi kan ikke anbefales pga. potentielle additive virkninger.
Hepatotoksicitet
- I kliniske studier (på andre indikationer og i højere doser) er der observeret leverenzymforstyrrelser specielt i løbet af de første 18 måneder af behandlingen. Stigningerne svandt gradvist efter seponering. Disse fund antyder, at tolvaptan muligvis kan forårsage irreversibel og potentielt dødelig leverskade.
- Ved tegn på leverskade, inklusiv træthed, anoreksi, ubehag i øverste højre del af abdomen, mørk urin eller gulsot, bør der straks tages leverfunktionsprøver.
- Ved mistanke om leverskade, skal tolvaptan omgående seponeres, passende behandling initieres, og undersøgelser iværksættes. Behandling bør kun genstartes, hvis det kan fastlægges, at årsagen til den observerede leverskade ikke har relation til tolvaptan-behandling.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Meget almindelige (> 10 %) | ||
| Mave-tarm-kanalen | Kvalme | |
| Metabolisme og ernæring | Tørst | |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Diarré, Mundtørhed, Obstipation | |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed, Temperaturstigning | |
| Undersøgelser | Forhøjet kreatinin i blodet | |
| Metabolisme og ernæring | Dehydrering, Hyperglykæmi, Hyperkaliæmi | Hypofagi |
| Nyrer og urinveje | Hyppig vandladning, Polyuri | |
| Hud og subkutane væv | Purpura | Hudkløe |
| Vaskulære sygdomme | Ortostatisk hypotension | |
| Ikke almindelige (0,1-1 %) | ||
| Mave-tarm-kanalen | Smagsforstyrrelser | |
| Nyrer og urinveje | Nyrefunktionspåvirkning | |
| Ikke kendt hyppighed | ||
| Immunsystemet | Anafylaktisk reaktion | |
| Hud og subkutane væv | Hududslæt | |
I kliniske undersøgelser på andre indikationer og i højere doser er forhøjede levertransaminaser, hypernatriæmi, hypoglykæmi, forhøjet serum-urat, synkope, svimmelhed, hovedpine, utilpashed og blod i urinen rapporteret som almindelige bivirkninger. Ikke almindeligt er set forhøjet bilirubin og kløende udslæt. Desuden akut leversvigt, hvor levertransplantation var påkrævet.
Kliniske aspekter
- De mest almindelige bivirkninger er tørst og kvalme.
- Tolvaptan medfører hos 5-10 % af patienterne en reversibel stigning i leverenzymer og bilirubin.
- Tolvaptan kan medføre irreversibel leverskade.
- Ved høj dosering, bør leverenzymer og bilirubin måles mindst én gang om måneden de første 18 behandlingsmåneder, herefter hver 3. måned.
- Hurtig reaktion på forhøjede leverenzymer kan reducere risikoen for leverskade.
- Tolvaptan kan forårsage hyperglykæmi og nedsat urinsyre-clearance.
Interaktioner
- Samtidig administration af moderate CYP3A-hæmmere, fx aprepitant, atazanavir, ciprofloxacin, crizotinib, darunavir/ritonavir, diltiazem, erythromycin, fosamprenavir, imatinib, verapamil, eller stærke CYP3A4-hæmmere, fx clarithromycin, ritonavir, ketoconazol og andre azoler, kan øge AUC for tolvaptan. Dosisreduktion af tolvaptan kan være nødvendigt.
- Forsigtighed ved samtidig administration af CYP3A-induktorer (fx rifampicin, rifabutin, phenytoin, barbiturater, carbamazepin og naturlægemidler med perikon), da de kan reducere AUC for tolvaptan med op til 87 %. Dosisøgning af tolvaptan kan blive nødvendig ved nedsat effekt.
- Samtidig behandling med lægemidler som er BCRP- , OCT1- eller P-glukoprotein -substrater, som hhv. sulfasalazin, metformin eller dabigatranexilat og digoxin, kan øge eksponering af disse substrater og dosisjustering kan være nødvendig. Større mængder (herunder som juice) af grapefrugt eller pomelo kan øge eksponeringen for tolvaptan 1,8 gange og bør undgås.
- Samtidig administration af tolvaptan og lægemidler, som har højt natriumindhold eller øger koncentrationen af serum-natrium, frarådes pga. risiko for hypernatriæmi.
- Samtidig behandling med vasopressinanaloger, fx desmopressin, frarådes.
Graviditet
Se også: Klassifikation - graviditet
Fertile kvinder og mænd
I produktresuméet anbefales, at kvinder i den fertile alder skal anvende sikker kontraception under behandlingen med tolvaptan. Denne anbefaling er baseret på en teoretisk vurdering af det aktive stofs egenskaber.
Amning
Bloddonor
Doping

|
Anvendelse af diuretika medfører diskvalifikation af den sportsudøvende både i og uden for konkurrence. |
Alkohol
Alkohol og Tolvaptan Accord påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Forgiftning
Der findes ingen specifik antidot. Tegn og symptomer på akut overdosering er overdrevne farmakologiske virkninger som stigning i serum-natrium, polyuri, tørst og dehydrering. Symptomatisk behandling.
Farmakodynamik
Selektiv vasopressin-receptorantagonist, som hæmmer virkningen af endogent vasopressin. Derved øges urinudskillelsen med øget aquaresis, nedsat urinosmolalitet og stigning i serum-natrium.
Farmakokinetik
- Biotilgængelighed ca. 56 %.
- Plasmahalveringstid ca. 8 timer.
- Metaboliseres i leveren.
- Mindre end 1 % udskilles uomdannet gennem nyrerne.
Holdbarhed og opbevaring
Holdbarhed
Opbevares i original emballage for at beskytte mod lys og fugt.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| tabletter | 7,5 mg |
Farve
Andre
|
|
| 15 mg |
Farve
Andre
|
||
| 30 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | tabletter
7,5 mg
(kan dosisdisp.)
Tolvaptan Accord |
568415 |
10 stk. (unit-dose)
|
6.496,80 | 649,68 | 2.598,72 | |
| (B) | tabletter
15 mg
(kan dosisdisp.)
Tolvaptan Accord |
508658 |
10 stk. (unit-dose)
|
9.086,80 | 908,68 | 1.817,36 | |
| (B) | tabletter
30 mg
(kan dosisdisp.)
Tolvaptan Accord |
100187 |
10 stk. (unit-dose)
|
6.496,80 | 649,68 | 649,68 |
Substitution
Foto og identifikation
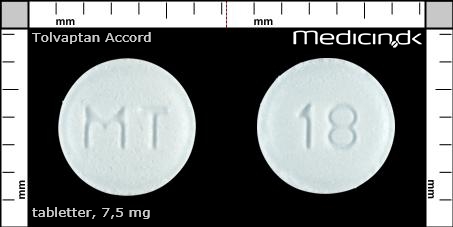
Tabletter 7,5 mg |
| Præg: |
MT, 18
|
| Kærv: | Ingen kærv |
| Farve: | Lyseblå |
| Mål i mm: | 5 x 5 |
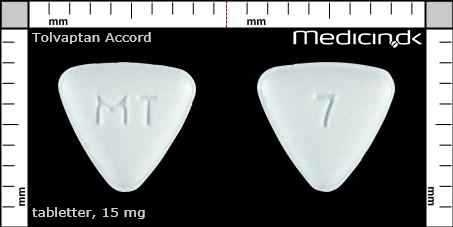
Tabletter 15 mg |
| Præg: |
MT, 7
|
| Kærv: | Ingen kærv |
| Farve: | Lyseblå |
| Mål i mm: | 6,7 x 6,3 |
Tabletter 30 mg |
| Præg: |
MT, 8
|
| Kærv: | Ingen kærv |
| Farve: | Lyseblå |
| Mål i mm: | 8,1 x 8,1 |

Referencer
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



