Yderligere information
Middel mod cystisk fibrose (CF), som indeholder en kombination af deutivacaftor/tezacaftor/vanzacaftor, der øger mængden af CFTR-protein og proteinets funktionalitet hos målgruppen.
Anvendelsesområder
Middel til behandling af Cystisk fibrose hos voksne og børn over 6 år, som har mindst én ikke-klasse I-mutation i CFTR-genet (cystic fibrosis transmembrane conductance regulator).
Behandlingen er en specialistopgave og bør forestås af læger med erfaring i behandling af cystisk fibrose.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder:
- 50 mg deutivacaftor, 20 mg tezacaftor og 4 mg vanzacaftor (som vanzacaftorcalciumdihydrat).
- 125 mg deutivacaftor, 50 mg tezacaftor og 10 mg vanzacaftor (som vanzacaftorcalciumdihydrat).
Doseringsforslag
Voksne, børn og unge ≥ 6 år
- Legemsvægt < 40 kg
3 tabletter (deutivacaftor 50 mg/tezacaftor 20 mg/vanzacaftor 4 mg) én gang dagligt. - Legemsvægt ≥ 40 kg
2 tabletter (deutivacaftor 125 mg/tezacaftor 50 mg/vanzacaftor 10 mg) én gang dagligt.
Kombination med CYP3A4-hæmmere
Dosis skal reduceres ved samtidig behandling med moderate CYP3A-hæmmere (fx. fluconazol, erythromycin, verapamil) eller potente CYP3A-hæmmere (fx ketoconazol, itraconazol, posaconazol, voriconazol eller clarithromycin):
Samtidig behandling med moderate CYP3A4-hæmmere:
- Legemsvægt < 40 kg
2 tabletter (deutivacaftor 50 mg/tezacaftor 20 mg/vanzacaftor 4 mg) hver anden dag. - Legemsvægt ≥ 40 kg
1 tablet (deutivacaftor 125 mg/tezacaftor 50 mg/vanzacaftor 10 mg) hver anden dag.
Samtidig behandling med potente CYP3A4-hæmmere:
- Legemsvægt < 40 kg
2 tabletter (deutivacaftor 50 mg/tezacaftor 20 mg/vanzacaftor 4 mg) én gang ugentligt. - Legemsvægt ≥ 40 kg
1 tablet (deutivacaftor 125 mg/tezacaftor 50 mg/vanzacaftor 10 mg) én gang ugentligt.
Bemærk:
- Patienten skal have CFTR genotypebestemt, før behandlingen startes.
- Bør tages på omtrent samme tidspunkt hver dag.
- Sikkerhed og virkning hos børn under 6 år er ikke klarlagt.
Børn og unge
-
Kontraindiceret, ingen eller begrænset erfaring
0-6 årSikkerhed og virkning hos børn under 6 år er ikke klarlagt.
Glemt medicin
- Ved under 6 timer efter det normale doseringstidspunkt tages den glemte dosis snarest muligt. Herefter fortsættes med den oprindelige doseringsplan dagen efter.
- Ved over 6 timer efter det normale doseringstidspunkt, skal den glemte dosis springes over, og behandlingen skal fortsættes efter den oprindelige doseringsplan dagen efter.
Håndtering
| filmovertrukne tabletter 125+50+10 mg |
| filmovertrukne tabletter 50+20+4 mg |
Knusning/åbning
Må ikke knuses.
Administration
Synkes hele.
Må ikke tygges.
Mad og drikke
Tages med fedtholdig mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
forsigtighed, ingen eller begrænset erfaring |
|
|---|---|
| GFR | Advarsel |
| <30 ml/min. |
Der er ingen erfaring hos patienter med svært nedsat nyrefunktion eller nyresygdom i slutstadiet. |
Nedsat leverfunktion
Let nedsat leverfunktion (Child-Pugh A)
- Der er ingen anbefaling om dosisjustering.
- Leverfunktionstest skal monitoreres tæt. Se under ”Forsigtighedsregler”.
Moderat nedsat lever funktion (Child-Pugh B)
- Anvendelse frarådes og må kun overvejes, når der er et klart lægeligt behov, og fordelen opvejer risikoen. I tilfælde af anvendelse er der ingen anbefaling om dosisjustering.
- Leverfunktionstest skal monitoreres tæt.
Stærkt nedsat leverfunktion (Child-Pugh C)
- Må ikke anvendes.
Forsigtighedsregler
Leverfunktionsprøver (ALAT/ASAT/bilirubin)
- Leverfunktionsprøver anbefales før behandlingen, hver 3. måned det første år og derefter årligt. Ved tidligere stigning i levertransaminaser bør hyppigere monitorering overvejes.
- Moderate stigninger i levertransaminaser er almindelige under behandlingen. Ved signifikante stigninger af levertransaminaser (fx ALAT/ASAT > 5 gange øvre normalgrænse eller ALAT/ASAT > 3 samt bilirubin > 2 gange øvre normalgrænse) bør behandlingen afbrydes, og patienten følges tæt til værdierne er normaliserede. Evt. fortsættelse af behandlingen kan derefter overvejes.
- Behandlingen skal afbrydes, og serumtransaminaser og total bilirubin skal straks måles, hvis en patient udvikler kliniske tegn eller symptomer på leverskade.
Organtransplanterede patienter
Bør undgås ved tidligere organtransplantation, da erfaring savnes.
Risiko for depression
Der er observeret depression og angst i forbindelse med behandlingen. Efter seponering er disse symptomer i nogle tilfælde bedret. Patienter (og omsorgspersoner) skal gøres opmærksom på behovet for overvågning af nedtrykt humør, selvmordstanker, søvnforstyrrelser eller usædvanlige ændringer i adfærd og kontakte læge, hvis disse symptomer forekommer.
Risiko for katarakt
Uklarheder i linsen er observeret hos pædiatriske patienter. Pga. mulig risiko for katarakt bør børn og unge under 18 år undersøges oftalmologisk før og efter behandlingsstart.
Bivirkninger
Dette lægemiddel har skærpet indberetningspligt. Alle eventuelle bivirkninger ved brugen skal derfor indberettes til Lægemiddelstyrelsen (Meld en bivirkning).
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Meget almindelige (> 10 %) | ||
| Mave-tarm-kanalen | Abdominalsmerter | Diarré |
| Infektioner og parasitære sygdomme | Infektion i øvre luftveje, Influenzalignende symptomer | |
| Undersøgelser | Forhøjede levertransaminaser | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Luftveje, thorax og mediastinum | Bakterier i sputum, Nasal tilstopning, Nasopharyngitis, Orofaryngeale smerter | |
| Almindelige (1-10 %) | ||
| Øre og labyrint | Tinnitus, Vestibulær sygdom, Øresmerter | Hyperæmi i trommehinden |
| Mave-tarm-kanalen | Kvalme | |
| Undersøgelser | Forhøjet ALAT/ASAT | Forhøjet plasma-kreatinkinase |
| Psykiske forstyrrelser | Angst, Depression | |
| Det reproduktive system og mammae | Knude i brystet | |
| Luftveje, thorax og mediastinum | Faryngalt erytem, Rhinitis, Sinuitis, Tilstoppede bihuler | |
| Hud og subkutane væv | Hududslæt | |
| Ikke almindelige (0,1-1 %) | ||
| Øre og labyrint | Trykken for ørerne | |
| Det reproduktive system og mammae | Brystinflammation, Gynækomasti | Ubehag i brystvorterne |
Kliniske aspekter
- De almindeligste bivirkninger hos personer med CF i alderen 12 år og ældre er hovedpine (16 %) og diarré (12 %).
- Der er rapporteret hududslæt. Hændelserne var lette i sværhedsgrad.
- Der er opstået forhøjet ALAT og forhøjet ASAT med hyppigheden 0,4 % under behandlingen. Monitorering af leverfunktionen anbefales derfor, som beskrevet under forsigtighedsregler. Patienten bør kontakte lægen ved symptomer på leverpåvirkning som bl.a. træthed, kvalme/opkastning, hudkløe/gulfarvning.
Interaktioner
CYP3A4: Kombination med induktorer og hæmmere
CYP3A-induktorer
- Vanzacaftor (VNZ), tezacaftor (TEZ) og deutivacaftor (D-IVA) er substrater for CYP3A. Samtidig anvendelse af CYP3A-induktorer kan medføre nedsat eksponering og dermed nedsat effekt af D-IVA/TEZ/VNZ. Administration samtidig med moderate eller potente CYP3A-induktorer anbefales ikke.
- Eksempler på moderate eller potente CYP3A-induktorer er rifampicin, rifabutin, phenobarbital, carbamazepin, phenytoin, prikbladet perikon og efavirenz.
CYP3A-hæmmere
- Administration samtidig med itraconazol, en potent CYP3A-hæmmer, øgede VNZ's AUC 10,5 gange, TEZ's AUC 4,0 til 4,5 gange og D-IVA's AUC 11,1 gange. D-IVA/TEZ/VNZ-dosen skal reduceres, når det anvendes samtidig med potente CYP3A-hæmmere.
- Eksempler på potente CYP3A-hæmmere er ketoconazol, itraconazol, posaconazol, voriconazol og clarithromycin.
- Eksempler på moderate CYP3A-hæmmere er fluconazol, erythromycin og verapamil.
- Administration af D-IVA/TEZ/VNZ samtidig med større mængder (herunder som juice) af grapefrugt eller pomelo, som indeholder en eller flere bestanddele, der i moderat grad hæmmer CYP3A, kan øge eksponeringen for VNZ, TEZ og D-IVA. Mad eller drikkevarer, der indeholder større mængder (herunder som juice) af grapefrugt eller pomelo, skal undgås under behandlingen.
Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
CYP2C9: Kombination med substrater
Ivacaftor kan hæmme CYP2C9. Forsigtighed ved kombination med midler, der metaboliseres via CYP2C9 (fx glimepirid, glipizid og visse benzodiazepiner), ligesom kontrol af INR anbefales ved kombination med warfarin.
Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
BCRP(brystcancerresistensprotein): Kombination med substrater
Vanzacaftor (VNZ), og deutivacaftor (D-IVA) hæmmer BCRP (brystcancerresistensprotein) in vitro. Forsigtighed ved samtidig behandling med substrater for BCRP (fx methotrexat, rosuvastatin, sulfasalazin).
OATP1B1: Kombination med substrater
Kan hæmme OATP1B1. Forsigtighed ved samtidig brug af substrater for OATP1B1 (fx statiner, enalapril, repaglinid, valsartan).
P-glykoprotein (P-gp): Kombination med substrater
Administration af D-IVA/TEZ/VNZ kan øge den systemiske eksponering for lægemidler, der er P-gp-substrater, hvilket kan øge eller forlænge deres terapeutiske virkning og bivirkninger. Ved administration samtidig med digoxin eller andre P-gp-substrater med et snævert terapeutisk indeks, som fx ciclosporin, everolimus, sirolimus og tacrolimus, skal der udvises forsigtighed og anvendes relevant monitorering.
Graviditet
Baggrund: Der er ikke humane data som tillader et meningsfyldt risikoestimat.
Se også: Klassifikation - graviditet
Amning
Baggrund: Der er ikke kvantitative data for udskillelse i modermælk.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Alyftrek® påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
- CFTR-proteinet er en anionkanal i cellemembranen, der regulerer cellernes vandbalance i de eksokrine kirtler. Cystisk fibrose skyldes en eller flere genetisk bestemte defekter i CFTR-proteinet - fx ukorrekt foldning og dermed hurtig nedbrydning af proteinet (den hyppigste årsag) eller ændringer i proteinet, som forhindrer normal transport af chlorid gennem kanalen.
- Kombinationen deutivacaftor/tezacaftor/vanzacaftor vil øge mængden af CFTR-protein og proteinets funktionalitet hos målgruppen.
Farmakokinetik
Vanzacaftor
- AUC øges 4 til 6 gange ved samtidig indtagelse af et fedtholdigt måltid.
- Steady state inden for 20 dage.
- Fordelingsvolumen ca 1,29 l/kg.
- Metaboliseres primært via CYP3A4/5. VNZ har ingen væsentlige cirkulerende metabolitter.
- Plasmahalveringstid ca. 10,1 timer.
Deutivacaftor
- AUC øges 3 til 4 gange ved samtidig indtagelse af fedtholdigt måltid.
- Steady state inden for 8 dage.
- Fordelingsvolumen ca. 2,25 l/kg.
- Metaboliseres primært via CYP3A4/5.
- Plasmahalveringstid ca. 2,67 timer.
Tezacaftor
- AUC påvirkes ikke af samtidig fødeindtagelse.
- Steady state inden for 8 dage.
- Fordelingsvolumen ca. 1,75 l/kg.
- Metaboliseres primært via CYP3A4/5.
- Plasmahalveringstid ca. 23,1 timer.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| filmovertrukne tabletter | 125+50+10 mg |
Deutivacaftor (125 mg)
Tezacaftor (50 mg)
Vanzacaftor (10 mg)
|
Farve
Andre
|
| 50+20+4 mg |
Deutivacaftor (50 mg)
Tezacaftor (20 mg)
Vanzacaftor (4 mg)
|
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (BEGR) | filmovertrukne tabletter
125+50+10 mg
(kan dosisdisp.)
Alyftrek |
551690 |
56 stk. (blister)
|
152.115,15 | 2.716,34 | ||
| (BEGR) | filmovertrukne tabletter
50+20+4 mg
(kan dosisdisp.)
Alyftrek |
471753 |
84 stk. (blister)
|
152.115,15 | 1.810,89 |
Foto og identifikation
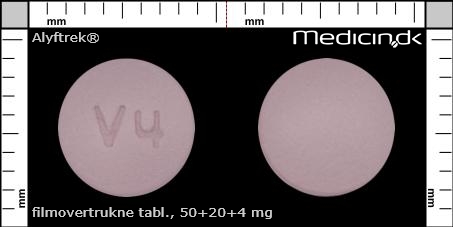
Filmovertrukne tabletter 50+20+4 mg |
| Præg: |
V4
|
| Kærv: | Ingen kærv |
| Farve: | Lilla |
| Mål i mm: | 7,4 x 7,4 |
Filmovertrukne tabletter 125+50+10 mg |
| Præg: |
V10
|
| Kærv: | Ingen kærv |
| Farve: | Lilla |
| Mål i mm: | 15 x 7 |

Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



