Yderligere information
Oralt lavdosis-kontraceptivum af kombinationstypen. Klassifikationen for denne p-pille er endnu uafklaret.
Anvendelsesområder
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 2 mg dienogest og 0,03 mg ethinylestradiol.
Doseringsforslag
I første behandlingsperiode startes på menstruationens 1. dag. Herved opnås sikker beskyttelse allerede fra 1. cyklusdag.
- Der tages 1 tabl. dgl. i 21 dage.
- Derefter 7 dages pause, hvori der kommer en menstruationslignende blødning.
Bemærk:
- Manglende erfaring vedr. behandling af patienter med let til moderat nedsat leverfunktion.
Børn og unge
-
Kontraindiceret, uegnet
0-13 årPræparatet er kun indiceret efter menarche.
Glemt medicin
Ved glemt p-pille følges nedenstående flowdiagram. Denne vejledning kan kun bruges, hvis der kun er glemt én p-pille i cyklus. Hvis der er glemt flere p-piller, indtages kun den sidst glemte og der skal anvendes anden prævention indtil start på næste p-pille pakning. Ved udebleven blødning i næste pause eller periode med inaktive tabletter bør der tages en graviditetstest.
- Dag 1 i grafikken viser den første dag, hvor der startes på en ny pakke p-piller.
- En grøn boks betyder, at beskyttelsen er som normalt, hvis den glemte p-pille tages og der følges eventuelle instrukser.
- En orange boks betyder, at beskyttelsen kan være nedsat, og at der derfor skal følges instrukser samt eventuelt bruge anden prævention i en periode.
- En rød boks betyder, at beskyttelsen er nedsat, og at graviditet kan være opstået hvis der har været samleje forud.
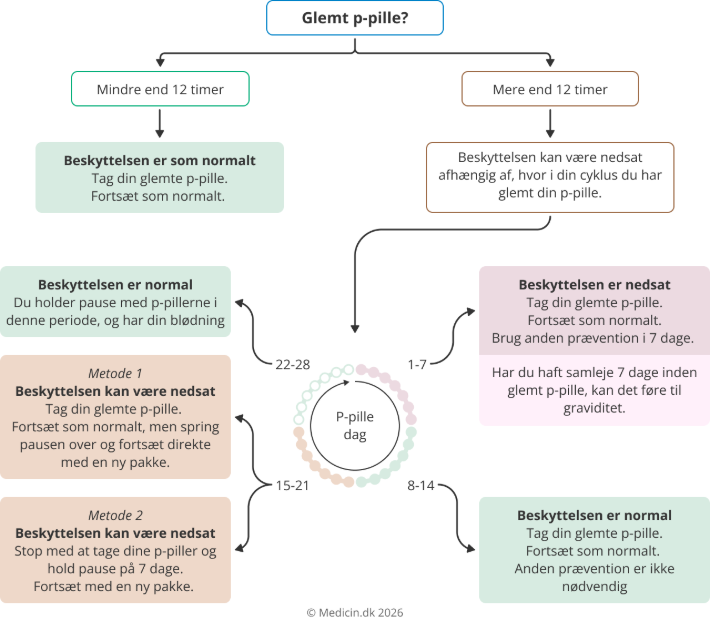
Se desuden Kombinationspræparater (hormonale kontraceptiva).
Håndtering
| filmovertrukne tabletter 2+0,03 mg |
Knusning/åbning
Må ikke knuses.
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
Kontraindikationer
- Aktuel eller tidligere venøs tromboemboli eller familiær disposition til dette (fx faktor V Leiden-mutation)
- Aktuel eller tidligere arteriel tromboembolisk sygdom (herunder TCI og angina pectoris)
- Alvorlige eller multiple risikofaktorer for venøs eller arteriel trombose
- Okulær lidelse af vaskulær oprindelse
- Migræne med fokale neurologiske symptomer
- Diabetes med vaskulære komplikationer
- Alvorlig hypertension
- Aktuel eller tidligere pancreatitis med alvorlig hypertriglyceridæmi
- Svær leversygdom
- Kønshormonafhængige maligne tilstande
- Tidligere eller nuværende levertumorer
- Uafklaret vaginalblødning.
Forsigtighedsregler
- Venøse tromboemboliske sygdomme
Kvinder med svær overvægt eller store åreknuder bør ikke anvende kontraception indeholdende ethinylestradiol. Ønsker man alligevel at give p-piller, må man foretrække midler med 2. generations gestagener. - Arterielle tromboemboliske sygdomme
Kontraception indeholdende ethinylestradiol bør ikke anvendes til kvinder over 35 år, som ryger, har hypertension eller andre kardiovaskulære risikofaktorer (fx svær dyslipoproteinæmi), idet risikoen for myokardieinfarkt og apopleksi øges. - Migræne
Patienter med migræne har formentlig en øget risiko for cerebral trombose, og p-piller bør derfor seponeres, hvis en kvinde udvikler migræne eller oplever forværring af eksisterende migræne under behandlingen. - Pausering i forbindelse med elektiv kirurgi
Det anbefales at seponere p-piller før større elektiv kirurgi, der kan forudses at medføre længerevarende immobilisering. I forbindelse med akut kirurgi kan det være en fordel at give tromboseprofylakse.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Nervesystemet | Hovedpine | |
| Det reproduktive system og mammae | Smerter i brysterne | |
| Ikke almindelige (0,1-1 %) | ||
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Kvalme, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed | |
| Undersøgelser | Vægtændring | |
| Metabolisme og ernæring | Hypofagi | |
| Knogler, led, muskler og bindevæv | Bækkensmerter | |
| Nervesystemet | Migræne, Svimmelhed | |
| Psykiske forstyrrelser | Humørforstyrrelser | |
| Det reproduktive system og mammae | Amenoré, Vaginitis | Brystspænding, Dysmenoré, Menstruationsforstyrrelser, Vaginal candidiasis, Vaginalt udflåd |
| Hud og subkutane væv | Alopeci | Acne, Hudkløe, Hududslæt |
| Vaskulære sygdomme | Hypertension, Hypotension | |
| Sjældne (0,01-0,1 %) | ||
| Blod og lymfesystem | Anæmi | |
| Hjerte | Kardiovaskulære hændelser | Takykardi |
| Øre og labyrint | Høretab (pludseligt), Tinnitus | |
| Det endokrine system | Virilisering | |
| Øjne | Synsforstyrrelser | Øjenirritation, Øjentørhed |
| Mave-tarm-kanalen | Gastritis, Gastroenteritis | |
| Almene symptomer og reaktioner på administrationsstedet | Cyster | Pyreksi |
| Immunsystemet | Psoriasis | |
| Infektioner og parasitære sygdomme | Infektion i nedre luftveje, Svampeinfektioner, Virale infektioner | Herpes labialis, Infektion i øvre luftveje, Influenzalignende symptomer |
| Metabolisme og ernæring | Hyperkolesterolæmi, Hypertriglyceridæmi, Lipomatose (i brystet) | |
| Knogler, led, muskler og bindevæv | Rygsmerter, Smerter i ekstremiteter | Muskuloskeletale smerter, Myalgi |
| Benigne, maligne og uspecificerede neoplasmer | Fibrocystisk brystsygdom, Forstørrelse af uterusfibromer, Ovariecyster | |
| Nervesystemet | Dystoni | |
| Psykiske forstyrrelser | Aggressivitet, Depression, Psykiske ændringer | Irritabilitet, Søvnforstyrrelser, Søvnløshed |
| Nyrer og urinveje | Cystitis, Urinvejsinfektion | |
| Det reproduktive system og mammae | Brystinflammation, Cervixdysplasi, Salpingitis, Underlivsbetændelse, Underlivssmerter | Dyspareuni, Galaktoré |
| Luftveje, thorax og mediastinum | Astma | Hyperventilation, Sinuitis |
| Hud og subkutane væv | Dermatitis, Eksem | Allergisk dermatitis, Chloasma, Hirsutisme, Hudlæsion, Hudreaktioner, Hyperpigmentering af huden, Seborré, Skæl, Øget svedtendens |
| Vaskulære sygdomme | Arterielle og venøse tromboembolier, Cerebral iskæmi, Cerebrovaskulære tilfælde, Dyb venetrombose, Iskæmi, Lungeemboli, Ortostatisk hypotension, Perifer vaskulær sygdom, Perifere ødemer, Tromboflebitis, Varicer | Hedeture |
| Ikke kendt hyppighed | ||
| Immunsystemet | Urticaria | |
| Traumer, forgiftninger og behandlingskomplikationer | Intolerance over for kontaktlinser | |
| Det reproduktive system og mammae | Blodigt sekret fra brystvorten, Nedsat libido, Øget libido | |
| Hud og subkutane væv | Erythema multiforme, Erythema nodosum | |
Kliniske aspekter
Risiko for tromboemboli
Brug af et kombineret hormonelt kontraceptivum øger risikoen for venøs tromboemboli (VTE), og i mindre grad for arteriel tromboemboli (ATE), sammenlignet med ingen anvendelse.
Risikoen for VTE er størst de første 6-12 måneder. Risikoen for tromboemboli stiger med alderen, mest udtalt for ATE.
Det bør sikres, at kvinden forstår risikoen. Se Hormonale kontraceptiva.
Androgene bivirkninger
Den vigtigste uønskede effekt er gestagenernes androgene virkning, der kan medføre acne (hos nogle ses dog en bedring pga. øget SHBG og nedsat frit androgen), kvalme og humørsvingninger.
Vægtøgning
I kontrollerede studier er der ikke påvist signifikant vægtøgning ved anvendelse af lavdosis p-piller.
Blødning
Blødningsproblemer ses hos helt op til 50 %, men forsvinder oftest efter de første 3 måneder. De ses hyppigere ved lavt hormonindhold og hos rygere.
Blødningsmængden reduceres i forhold til normal menstruation og nogle få procent vil opleve amenoré. Tilstanden er ufarlig, men kan give bekymring om graviditet.
Depression
Der er påvist en sammenhæng mellem brug af gestagen og start på antidepressiva. Dette gælder specielt for kvinder under 25 år og det er vigtigt at screene for depressive symptomer.
Brystkræft
Risikoen for brystkræft synes at øges med en relativ risiko på 1,2 ved anvendelse af kombinerede kontraceptiva. Den absolutte risikoforøgelse er dog lille. Se Hormonale kontraceptiva.
Anvendelse af p-piller af kombinationstypen er desuden forbundet med:
- Kvalme, brystspænding og vægtstigning, som er mest udtalte i starten og som regel forsvinder ved fortsat brug.
- Benigne levertumorer (fx fokal nodulær hyperplasi, leveradenom)
- Leverpåvirkning (fx hepatitis, nedsat leverfunktion)
- Let øget risiko for cervixkarcinom (ved eksisterende HPV-infektion)
- Opticus neuritis og retinal blodprop
- Forværring af åreknuder
- Udvikling af chloasma i ansigtet
- Pancreatitis med samtidig hypertriglyceridæmi
- Iskæmisk colitis
- Øget risiko for galdestenssymptomer
- Forværring af porfyri
- Forværring af systemisk lupus erythematosus
- Kroniske inflammatoriske tarmsygdomme
- Forværring af chorea minor (Sydenhams korea)
- Udvikling eller forværring af symptomer ved hereditært eller erhvervet angioødem
- Otosklerose
- Hæmolytisk-uræmisk syndrom.
Interaktioner
CYP3A4 induktorer og hæmmere
Hormonale kontraceptiva metaboliseres bl.a. via CYP3A4 og kombination med induktorer og hæmmere af dette enzym kan påvirke omsætningen.
- Induktorer af CYP3A4 kan øge metaboliseringshastigheden, hvilket kan medføre gennembrudsblødning eller nedsat antikonceptionel virkning. CYP3A4-induktorer er fx visse antiepileptika (bl.a phenytoin, carbamazepin, perampanel, topiramat), visse antibiotika (bl.a. rifampicin, rifabutin), bosentan, modafinil, nevirapin og naturlægemidler indeholdende perikon - se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
- Potente hæmmere af CYP3A4 kan øge plasmakoncentration. Dette kan muligvis øge risikoen for bivirkninger. Potente hæmmere er fx azol-antimykotika (voriconazol mm.), verapamil, makrolider (fx clarithromycin, erythromycin), diltiazem og større mængder (herunder som juice) af grapefrugt eller pomelo - se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
Proteasehæmmere
Der er set øget metabolisme og reduktion af plasmakoncentrationen af hormonelle kontraceptiva og ritonavir. Sandsynligvis via øget glukuronidering. Risiko for gennembrudsblødning og nedsat antikonceptionel virkning. Flere andre proteasehæmmere kan desuden i varierende grad påvirke metaboliseringen af hormonelle kontraceptiva gennem påvirkning af CYP3A4. Alternativ kontraceptionsmetode bør overvejes.
CYP3A4 substrater
Metaboliseringen af visse andre CYP3A4 substrater kan nedsættes (muligvis pga. kompetitiv hæmning). Dosisjustering kan være nødvendig. Det gælder bl.a. ciclosporin. Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
CYP1A2 og CYP2C19 substrater
Ethinylestradiol hæmmer CYP1A2 og CYP2C1, hvilket kan føre til øget plasmakoncentration for substrater af disse enzymer. Det gælder bl.a. clozapin og tizanidin, hvor dosisjustering kan være nødvendig. Se endvidere tabel 2 i Elimination og cytokrom P450-systemet.
Colesevelam
Colesevelam i kombination med orale hormonelle kontraceptiva nedsætter biotilgængeligheden af ethinylestradiol. P-piller bør derfor indtages mindst 1 time før eller 4 timer efter colesevelam.
Etoricoxib
Etoricoxib øger plasmakoncentrationen af ethinylestradiol pga. hæmning af sulfotransferaseaktiviteten. Risikoen for bivirkninger, bl.a. venøs tromboemboli, hos disponerede kvinder, kan muligvis øges.
Glukokortikoider
Hormonale kontraceptiva kan øge virkningen af glukokortikoider. Muligvis pga. en øgning af kortisol bindende globulin og følgende nedsat clearance. Dosisjustering kan være nødvendig.
Lamotrigin
Plasmakoncentrationen af lamotrigin nedsættes ved brug af hormonale kontraceptiva pga. øget glukuronidering. Dosisjustering og kontrol af plasmakoncentration kan være nødvendig.
Levothyroxin
Østrogenbehandling kan medføre reduktion af frit thyroxin samt øgning af TSH hos hypothyroide kvinder i behandling med levothyroxin. Dosisjustering kan være nødvendig.
Midler til behandling af hepatitis C
Der er set forhøjet niveau af ALAT (over 5 gang øverste normalgrænse) ved samtidig behandling med ethinylestradiol og en række antivirale midler mod hepatitis C. Det gælder glecaprevir/pibrentasvir og sofosbuvir/velpatasvir/voxilaprevir, hvor kombination med ethinylestradiol er kontraindiceret (indtag af midler indeholdende ethinylestradiol kan genoptages 2 uger efter afsluttet behandling med de antivirale midler).
Graviditet
Baggrund: Der er data for mange tusinde børn, der er blevet eksponerede for p-piller i 1. trimester uden betydende overhyppighed af misdannelser. Konstateres graviditet, skal behandlingen afbrydes.
Se også: Klassifikation - graviditet
Amning
Baggrund: Der er ingen data for udskillelse af dienogest i modermælk. Den relative vægtjusterede dosis for estradiolvalerat er under 1 %, hvilket er betryggende lavt.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Yana® påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
P-piller af kombinationstypen virker ved at nedsætte sekretionen af gonadotropin, hvilket hæmmer ovulationen, samt ved at reducere proliferationen af endometrium og forårsage en fortykkelse af slimen i cervix, så den dermed bliver uigennemtrængelig for sædceller.
Farmakokinetik
Ethinylestradiol
- Biotilgængelighed ca. 45 % pga. first pass-metabolisme i tarm og lever.
- Eliminationen er bifasisk med terminal plasmahalveringstid på 24 timer.
- Udskilles som metabolitter gennem nyrerne og med fæces.
Dienogest
- Biotilgængelighed ca. 91 %.
- Plasmahalveringstid ca. 11 timer.
- Udskilles gennem nyrerne og med fæces.
Klima og miljø
Miljøpåvirkning
Dienogest og ethinylestradiol udgør en risiko for vandmiljøet. Særlig opmærksomhed på korrekt bortskaffelse af evt. ikke-anvendt lægemiddel.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| filmovertrukne tabletter | 2+0,03 mg |
Dienogest (2 mg)
Ethinylestradiol (,03 mg)
|
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | filmovertrukne tabletter
2+0,03 mg
Yana |
555222 |
63 stk. (blister)
|
223,75 | 3,55 |
Foto og identifikation
Filmovertrukne tabletter 2+0,03 mg |
| Præg: |
Intet præg
|
| Kærv: | Ingen kærv |
| Farve: | Hvid |
| Mål i mm: | 6 x 6 |

Referencer
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
4098. Charlton BM, Mølgaard-Nielsen D, Svanström H et al. Maternal use of oral contraceptives and risk of birth defects in Denmark: prospective, nationwide cohort study. BMJ. 2016, https://pubmed.ncbi.nlm.nih.gov/26738512/ (Lokaliseret 22. marts 2026)
4099. Wogelius P, Horváth-Puhó E, Pedersen L et al. Maternal use of oral contraceptives and risk of hypospadias - a population-based case-control study. Eur J Epidemiol. 2006; 21(10):777-81, https://pubmed.ncbi.nlm.nih.gov/17077991/ (Lokaliseret 22. marts 2026)
4100. Raman-Wilms L, Tseng AL, Wighardt S et al. Fetal genital effects of first-trimester sex hormone exposure: a meta-analysis. Obstet Gynecol. 1995; 85(1):141-9, https://pubmed.ncbi.nlm.nih.gov/7800312/ (Lokaliseret 22. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



