Yderligere information
Antiviralt middel. Hæmmer funktionen af det HIV-kodede enzym integrase.
Anvendelsesområder
- Infektion med HIV-1 hos voksne, børn og unge med legemsvægt ≥ 40 kg.
- Anvendes til behandlingsnaive patienter eller patienter, der blev virologisk supprimerede i initial behandling med 400 mg.
Til børn < 6 år og/eller med legemsvægt < 25 kg findes tyggetabletter og granulat til oral suspension, som kan rekvireres med udleveringstilladelse fra lægemiddelstyrelsen, se Dosering.
Se kombinationsbehandling i Midler mod HIV.
Bør kun anvendes, når behandlingen forestås af læger med særlig indsigt i HIV-associerede sygdomme og deres behandling.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 600 mg raltegravir.
Doseringsforslag
- Voksne og børn med legemsvægt ≥ 40 kg
- 1.200 mg (2 tbl. á 600 mg) 1 gang dgl.
- Bemærk: 400 mg tabletter må ikke anvendes til denne dosering.
Bemærk:
- Tabletter og tyggetabletter/oral suspension er ikke bioækvivalente.
- Erfaring savnes vedr. børn med legemsvægt < 40 kg.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-6 årErfaring savnes med tabletter ved behandling af børn med legemsvægt under 25 kg (hvilket svarer til en alder på under 6 år). Der findes tyggetabletter og oral suspension til mindre børn; men de er ikke markedsførte og kan derfor kun rekvireres med udleveringstilladelse fra Lægemiddelstyrelsen. Bemærk, at tyggetabletter og oral suspension ikke er bioækvivalente med tabletterne.
Håndtering
| filmovertrukne tabletter 600 mg |
Knusning/åbning
Kan knuses.
Bemærk: Knusning kan nedsætte/øge virkningen af tabletterne, og derfor er ekstra kontrol nødvendigt.
Administration
Knust tablet kan opslæmmes i vand.
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på en skefuld kold, blød mad, fx yoghurt eller æblemos.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
Forsigtighedsregler
- Stærkt nedsat leverfunktion (Child-Pugh C). Leverfunktionen bør kontrolleres jævnligt.
- Ved alvorligt hududslæt, mistanke om DRESS syndrom (Drug Rash med Systemiske Symptomer) eller alvorlige allergiske reaktioner skal raltegravir omgående seponeres.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Blod og lymfesystem | Abnorm lymfocyt-morfologi | |
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Flatulens, Kvalme, Meteorisme, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed, Temperaturstigning, Træthed | |
| Undersøgelser | Forhøjet ALAT/ASAT | Forhøjet plasma-amylase, Forhøjet plasma-kreatinkinase, Forhøjet plasma-lipase |
| Metabolisme og ernæring | Hypofagi | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Psykiske forstyrrelser | Depression, Hyperaktivitet | Abnorme drømme, Mareridt, Søvnløshed |
| Hud og subkutane væv | Hudkløe, Hududslæt | |
| Ikke almindelige (0,1-1 %) | ||
| Blod og lymfesystem | Anæmi, Neutropeni, Trombocytopeni | Hævede lymfeknuder, Smerter i lymfeknuder |
| Hjerte | Myokardieinfarkt, Ventrikulær ekstrasystoli | Palpitationer |
| Øre og labyrint | Tinnitus | |
| Øjne | Synsforstyrrelser | |
| Mave-tarm-kanalen | Odynofagi, Pancreatitis, Rektal blødning | Gastritis, Gastroenteritis, Gastro-øsofageal refluks, Gingivitis, Glossitis, Mundtørhed, Obstipation, Smagsforstyrrelser |
| Almene symptomer og reaktioner på administrationsstedet | Letargi, Smerter | Kulderystelser / kuldegysninger, Utilpashed |
| Lever og galdeveje | Hepatitis, Leverinsufficiens | |
| Immunsystemet | Ansigtsødem, Hypersensitivitet, Immunrekonstitutionsinflammatorisk syndrom, Stevens-Johnsons syndrom | Urticaria |
| Infektioner og parasitære sygdomme | Herpes zoster | Infektion i øvre luftveje, Influenzalignende symptomer |
| Traumer, forgiftninger og behandlingskomplikationer | Tendinitis | |
| Undersøgelser | Forhøjet bilirubin, Forhøjet INR, Glucosuri | Forhøjet plasma-carbamid og -kreatinin, Vægtøgning |
| Metabolisme og ernæring | Diabetes, Dyslipidæmi, Hyperglykæmi, Hyperkolesterolæmi | Hypoalbuminæmi, Lipodystrofi |
| Knogler, led, muskler og bindevæv | Artralgi, Knoglesmerter, Osteopeni, Rhabdomyolyse, Rygsmerter, Smerter i ekstremiteter | Myalgi, Nakkesmerter |
| Benigne, maligne og uspecificerede neoplasmer | Papillom | |
| Nervesystemet | Hukommelsesbesvær, Hypæstesi, Karpaltunnelsyndrom, Migræne, Perifer neuropati, Tremor | |
| Psykiske forstyrrelser | Angst, Kognitiv dysfunktion, Konfusion, Selvmordsadfærd | Døsighed, Søvnforstyrrelser |
| Nyrer og urinveje | Hæmaturi, Kronisk nyresygdom, Nefritis, Nefrotisk syndrom | Nykturi |
| Det reproduktive system og mammae | Erektil dysfunktion, Genital herpes simplex, Gynækomasti | Menopausale symptomer, Ubehag i brysterne |
| Luftveje, thorax og mediastinum | Dysfoni | Epistaxis, Nasal tilstopning, Nasopharyngitis |
| Hud og subkutane væv | Alopeci, Dermatitis, Folliculitis, Lægemiddelreaktion med eosinofili og systemiske symptomer - DRESS | Acne, Øget svedtendens |
| Vaskulære sygdomme | Hypertension, Perifere ødemer | Hedeture |
Kliniske aspekter
- De hyppigste bivirkninger var hovedpine, kvalme og abdominalsmerter. De hyppigst rapporterede, alvorlige bivirkninger var immunreaktiveringssyndrom og udslæt. Hyppigheden for seponering af raltegravir på grund af bivirkninger var 5% eller mindre i kliniske studier.
- Bivirkningen rhadomyolyse blev rapporteret med hyppigheden ikke almindelig i forbindelse med brug af raltegravir 400 mg to gange dagligt efter markedsføring.
- Alvorlige, potentielt livstruende og letale hudreaktioner er set, ofte ved samtidig indtagelse af andre lægemidler.
- Depression og selvmordstanker ses især hos patienter, som har eller tidligere har haft psykisk sygdom.
- Vedr. metaboliske bivirkninger under antiretroviral kombinationsbehandling, se Midler mod HIV.
Interaktioner
- Samtidig administration af potente induktorer af UGT1A1, fx rifampicin, kan reducere plasmakoncentrationen af raltegravir. Hvis kombinationen er absolut nødvendig, bør det overvejes at fordoble raltegravir dosis.
- Hæmmere af UGT1A1, fx atazanavir eller omeprazol, kan øge plasmakoncentrationen af raltegravir. Dosisjustering ikke nødvendig.
- Samtidig administration af aluminium- eller magnesiumholdige antacida reducerer plasmakoncentrationen af raltegravir. Derfor frarådes kombination.
- Jernsalte forventes at nedsætte plasmakoncentrationen af raltegravir; men denne virkning kan begrænses ved administrering af jernsalte mindst 2 timer før eller efter indtagelse af raltegravir.
Graviditet
Baggrund: Store epidemiologiske studier viser samstemmende, at antiretroviral behandling under graviditeten (for alle lægemidler og kombinationer er der data for i alt > 35.000 gravide; heraf > 16.000 eksponeret i 1. trimester) ikke er forbundet med en overhyppighed af medfødte misdannelser. Visse studier viser en lidt øget risiko for tidlig fødsel og lav fødselsvægt, men det er uklart, om og i hvilket omfang dette kan tilskrives behandlingen.
For raltegravir er der data for ca. 250 1. trimester eksponerede uden tegn på overhyppighed af uønsket fosterpåvirkning.
Behandling af gravide med HIV-infektion er en specialistopgave. Se endvidere Midler mod HIV.
Se også: Klassifikation - graviditet
Amning
Baggrund: Amning frarådes på grund af smitterisiko.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Forsigtighed ved indtagelse af alkohol under behandling med Raltegravir "Zentiva".
Alkoholforbrug kan bidrage til tilfælde af osteonekrose.
Farmakodynamik
- HIV-integrasehæmmer.
- Hindrer den kovalente integration af HIV-genomet i værtsgenomet og dermed udbredelse af virusinfektionen.
Farmakokinetik
- Ca. 10 % udskilles uomdannet gennem nyrerne.
- Plasmahalveringstid ca. 9 timer.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| filmovertrukne tabletter | 600 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (BEGR) | filmovertrukne tabletter
600 mg
(kan dosisdisp.)
Raltegravir "Zentiva" |
497695 |
60 stk.
|
5.978,80 | 99,65 | 132,86 |
Substitution
| filmovertrukne tabletter 600 mg |
|---|
| Isentress MSD, Raltegravir, filmovertrukne tabletter 600 mg |
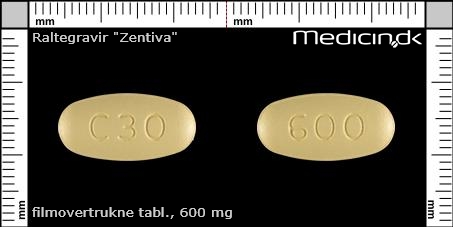
Foto og identifikation
Filmovertrukne tabletter 600 mg |
| Præg: |
C30, 600
|
| Kærv: | Ingen kærv |
| Farve: | Gul |
| Mål i mm: | 9,3 x 19 |
Referencer
4375. Gandhi RT, Bedimo R, Hoy JF et al. Antiretroviral Drugs for Treatment and Prevention of HIV Infection in Adults: 2022 Recommendations of the International Antiviral Society-USA Panel. JAMA. 2023; 329-(1):63-84, https://pubmed.ncbi.nlm.nih.gov/33052386/ (Lokaliseret 25. marts 2026)
4376. European Pregnancy and Paediatric HIV Cohort Collaboration (EPPICC) Study Group. Nucleoside reverse transcriptase inhibitor backbones and pregnancy outcomes. AIDS. 2019; 33(2):295-304, https://pubmed.ncbi.nlm.nih.gov/30562172/ (Lokaliseret 25. marts 2026)
4377. Veroniki AA, Antony J, Straus SE et al. Comparative safety and effectiveness of perinatal antiretroviral therapies for HIV-infected women and their children: Systematic review and network meta-analysis including different study designs. PLoS One. 2018; 13(6), https://pubmed.ncbi.nlm.nih.gov/29912896/ (Lokaliseret 25. marts 2026)
4379. Rough K, Seage GR 3rd, Williams PL et al. Birth Outcomes for Pregnant Women with HIV Using Tenofovir-Emtricitabine. N Engl J Med. 2018; 378(17):1593-603, https://pubmed.ncbi.nlm.nih.gov/29694825/ (Lokaliseret 25. marts 2026)
4378. Zash R, Jacobson DL, Diseko M et al. Comparative Safety of Antiretroviral Treatment Regimens in Pregnancy. JAMA Pediatr. 2017; 171(10), https://pubmed.ncbi.nlm.nih.gov/28783807/ (Lokaliseret 25. marts 2026)
4374. Antiretroviral Pregnancy Registry Advisory Committee. Interim Report. ANTIRETROVIRAL PREGNANCY REGISTRY. 1989-2023, https://www.apregistry.com/InterimReport.aspx (Lokaliseret 25. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



