Antihypertensivum og middel mod hjerteinsufficiens. Hæmmer Angiotensin Converting Enzyme (ACE).
Anvendelsesområder
- Arteriel hypertension.
- Venstresidig Hjerteinsufficiens med reduceret pumpefunktion.
- Nedsat venstre ventrikelfunktion og/eller kliniske tegn på hjertesvigt efter AMI.
- Forsinkelse af udvikling og progression af diabetisk nefropati samt visse andre kroniske nefropatiformer med proteinuri.
Dispenseringsform
Tabletter. 1 tablet indeholder 12,5 mg (delekærv), 25 mg (krydskærv) eller 50 mg (krydskærv) captopril.
Doseringsforslag
Arteriel hypertension
- Initialt 25-50 mg dgl. fordelt på 2 doser. Afhængig af effekt kan dosis øges til maksimalt 150 mg dgl.
- Doser større end 100 mg dgl. er dog sjældent nødvendig.
- Ved samtidig diuretisk terapi gives initialt 25 mg dgl., alternativt seponeres diuretikumbehandlingen 3 døgn, før captoprilbehandlingen indledes.
Hjerteinsufficiens
- Initialt 6,25 mg 2 gange dgl. stigende efter effekt til 25-50 mg 2 gange dgl. under nøje kontrol af især blodtrykket.
Nedsat uddrivningsfraktion efter akut myokardieinfarkt
- Initialt 6,25 mg 1-2 gange dgl., evt. stigende gradvis til 25 mg 3 gange dgl.
Forebyggelse af nefropati hos patienter med type 1 diabetes
- 75-100 mg dgl. fordelt på 2 doser.
Bemærk:
- Ældre. Initialt 6,25 mg 2 gange dgl.
- Børn og unge. Initialt ca. 0,3 mg/kg legemsvægt under tæt medicinsk overvågning.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-17 årErfaring savnes ved behandling af børn og unge under 17 år. Initialt anbefales ca. 0,3 mg/kg under tæt medicinsk overvågning.
Håndtering
| tabletter 12,5 mg |
| tabletter 25 mg |
| tabletter 50 mg |
Knusning/åbning
Kan knuses.
Administration
Synkes hele, halve eller kvarte.
Tablet eller knust tablet kan opslæmmes i vand.
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på kold, blød mad.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
forsigtighed, dosisjustering |
||
|---|---|---|
| GFR | Alder | Advarsel |
| <10 ml/min. | ≥17 år |
Initialdosis 6,25 mg dgl. Højst 37,5 mg dgl. Rutinemæssig monitorering af P-kalium og P-kreatinin. |
| 10-20 ml/min. | ≥17 år |
Initialdosis 12,5 mg dgl. Højst 75 mg dgl. Rutinemæssig monitorering af P-kalium og P-kreatinin. |
| 10-50 ml/min. | 2-17 år |
Initialdosis 0,15 mg/kg under tæt overvågning. Højst 3 mg/kg legemsvægt dgl. fordelt på 3 doser. |
| 20-40 ml/min. | ≥17 år |
Initialdosis 25 mg dgl. Højst 100 mg dgl. Rutinemæssig monitorering af P-kalium og P-kreatinin. |
Nedsat leverfunktion
- Forhøjet plasmakoncentration er set ved levercirrose.
- Ved let til moderat nedsat leverfunktion bør dosisnedsættelse overvejes.
Kontraindikationer
- Tidligere forekomst af angioneurotisk ødem under behandling med ACE-hæmmere.
- Der er krydsallergi med øvrige ACE-hæmmere.
- Samtidig behandling med aliskiren til patienter med diabetes eller nedsat nyrefunktion, GFR < 60 ml/min.
- Samtidig behandling med sacubitril/valsartan pga. øget risiko for angioødem.
Forsigtighedsregler
- Arvelig eller idiopatisk angioødem
- Mitralklapstenose
- Aortastenose
- Hypertrofisk kardiomyopati
- Nyrearteriestenose
- Bindevævssygdomme og tilstande med leuko- og trombocytopeni pga. risiko for udvikling af alvorlige infektioner.
- En evt. hyponatriæmi og hypovolæmi bør korrigeres før behandlingen indledes.
- Ekstrakorporal behandling, der fører til blodkontakt med negativt ladede overflader pga. risiko for udvikling af anafylaktiske reaktioner.
- Efter de første doser kan der komme et udtalt blodtryksfald. Risikoen er størst ved samtidig behandling med diuretika og/eller andre vasodilatorer.
Bivirkninger
Hoste er den hyppigste bivirkning og hos 5-10 % af patienterne så generende, at behandlingen må seponeres.
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Kvalme, Mundtørhed, Obstipation, Opkastning, Smagsforstyrrelser |
| Nervesystemet | Svimmelhed | |
| Psykiske forstyrrelser | Søvnforstyrrelser | |
| Luftveje, thorax og mediastinum | Dyspnø | Hoste |
| Hud og subkutane væv | Alopeci | Hudkløe, Hududslæt |
| Ikke almindelige (0,1-1 %) | ||
| Hjerte | Angina pectoris | Palpitationer, Takykardi |
| Almene symptomer og reaktioner på administrationsstedet | Træthed | |
| Immunsystemet | Angioødem | |
| Det reproduktive system og mammae | Smerter i brysterne | |
| Hud og subkutane væv | Rødme | |
| Vaskulære sygdomme | Hypotension, Raynauds syndrom | |
| Sjældne (0,01-0,1 %) | ||
| Metabolisme og ernæring | Hypofagi | |
| Nervesystemet | Paræstesier | Hovedpine |
| Psykiske forstyrrelser | Døsighed | |
| Nyrer og urinveje | Nyrefunktionspåvirkning | |
| Meget sjældne (< 0,01 %) | ||
| Blod og lymfesystem | Agranulocytose, Anæmi, Eosinofili, Trombocytopeni | |
| Hjerte | Hjertestop | |
| Øjne | Sløret syn | |
| Mave-tarm-kanalen | Gastro-duodenale ulcera, Pancreatitis | |
| Almene symptomer og reaktioner på administrationsstedet | Pyreksi | |
| Lever og galdeveje | Hepatitis, Leverpåvirkning | |
| Immunsystemet | Stevens-Johnsons syndrom | Urticaria |
| Undersøgelser | Forhøjet plasma-carbamid og -kreatinin | |
| Metabolisme og ernæring | Hyperkaliæmi, Hypoglykæmi, Hyponatriæmi | |
| Knogler, led, muskler og bindevæv | Artralgi | Myalgi |
| Psykiske forstyrrelser | Depression, Konfusion | |
| Nyrer og urinveje | Nefrotisk syndrom | |
| Det reproduktive system og mammae | Gynækomasti, Impotens | |
| Luftveje, thorax og mediastinum | Bronkospasme, Eosinofil pneumoni | Rhinitis |
| Hud og subkutane væv | Bulløs pemfigoid, Eksfoliativ dermatitis, Erythema multiforme, Fotosensibilitet | |
| Vaskulære sygdomme | Cerebrovaskulære tilfælde, Synkope | |
Kliniske aspekter
- Tør, irritativ hoste bedres ikke ved skift til en anden ACE-hæmmer. Skift til angiotensin II- antagonist afhjælper oftest problemet.
- Risiko for udtalt blodtryksfald er registreret hos patienter med stærkt aktiveret renin-angiotensin-aldosteron system, især i starten af behandling. Lavere startdosis kan anvendes og/eller brug af præparater med længere halveringstid.
- I I tilfælde af angioneurotisk ødem er skift til anden ACE-hæmmer kontraindiceret, og man skal være varsom ved skift til angiotensin II-antagonist.
- Hyperkaliæmi er især set hos ældre (> 70 år) ved samtidig behandling med kaliumbesparende diuretika/aldosteron antagonister og/eller nedsat nyrefunktion. Kontrol af p-kalium anbefales hos disse patienter.
- Captopril benyttes sjældent til behandling pga. captoprils korte halveringstid.
Interaktioner
- Samtidig behandling med aliskiren er kontraindiceret til patienter med diabetes eller nedsat nyrefunktion, GFR < 60 ml/min.
- Samtidig behandling med sacubitril/valsartan er kontraindiceret pga. øget risiko for angioødem. Behandling med sacubitril/valsartan må ikke indledes før mindst 36 timer efter sidste dosis captopril, og behandling med captopril må ikke indledes før mindst 36 timer efter den sidste dosis sacubitril/valsartan.
- Samtidig anvendelse af angiotensin II-receptorantagonist eller aliskiren (dobbelthæmning af renin-angiotensin-aldosteronsystemet) øger risikoen for hypotension, hyperkaliæmi og nedsat nyrefunktion.
- Ved samtidig indgift af kalium eller kaliumbesparende diuretika øges kaliumkoncentrationen i blodet pga. ACE-hæmmernes aldosteronsekretionshæmmende virkning.
- Der er risiko for lithiumintoksikation ved samtidig indgift af lithium. Serum-lithium bør kontrolleres.
- Samtidig behandling med trimethoprim/sulfamethoxazol eller ciclosporin kan øge risikoen for hyperkaliæmi. Serum-kalium bør følges.
- Samtidig behandling med allopurinol kan udløse alvorlige overfølsomhedsreaktioner.
- NSAID (inkl. ASA > 300 mg/døgn) kan reducere den antihypertensive effekt af ACE-hæmmere og øge risikoen for nyrefunktionsnedsættelse.
- Det er uafklaret, om ACE-hæmmere øger insulinfølsomheden og kan medføre hypoglykæmi ved samtidig behandling med antidiabetika. Hyppig måling af blodsukkeret ved indledning og ophør af kombinationsbehandling anbefales.
- Der er øget risiko for angioødem ved samtidig behandling med mTOR-hæmmere (fx everolimus og sirolimus).
Graviditet
Baggrund:
Risikoen for uønsket fosterpåvirkning ved 1. trimester eksponering for ACE-hæmmere generelt er let forhøjet sammenlignet med baggrundsrisikoen til omkring 5-6 %. Sammenlignet med ubehandlet hypertension (og justeret for andre faktorer) synes risikoen imidlertid uændret.
Må ikke anvendes i 2. og 3. trimester af graviditeten på grund af øget risiko for uønsket fosterpåvirkning, specielt i form af væksthæmning, hypocalvaria, oligohydramnios, neonatal anuri, neonatal hypotension og persisterende ductus arteriosus.
De forskellige studier omfatter sammenlagt mere end 6.700 gravide eksponeret for en ACE-hæmmer i 1. trimester af graviditeten, heraf mindre end 150 for captopril.
Se endvidere ACE-hæmmere.
Det anbefales fortsat at skifte behandlingen til et af de rekommanderede præparater; se Hypertension hos gravide.
Se også: Klassifikation - graviditet
Amning
Baggrund: Den relative vægtjusterede dosis er under 1 %. Der er ikke beskrevet bivirkninger hos barnet.
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Captopril "Stada" påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Farmakodynamik
- Hæmmer enzymet ACE og dermed omdannelsen af angiotensin I til II, hvorved universel vasodilatation indtræder.
- Virkningen indtræder efter ca. 15 minutter og er maksimal efter 1-1,5 timer.
Farmakokinetik
- Ca. 60 % absorberes fra mave-tarm-kanalen. Samtidig fødeindtagelse nedsætter absorptionsfraktionen med ca. 30 %.
- Maksimal plasmakoncentration efter 0,5-1,5 timer.
- Metaboliseres delvis i leveren.
- Plasmahalveringstid ca. 2 timer.
- Ca. 50 % udskilles uomdannet gennem nyrerne.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| tabletter | 12,5 mg |
Andre
|
|
| 25 mg |
Andre
|
||
| 50 mg |
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | tabletter
12,5 mg
(PharmaCoDane)
(kan dosisdisp.)
Captopril "Stada" |
023827 |
100 stk. (blister)
|
279,50 | 2,80 | 11,18 | |
| (B) | tabletter
25 mg
(PharmaCoDane)
(kan dosisdisp.)
Captopril "Stada" |
023808 |
100 stk. (blister)
|
300,25 | 3,00 | 6,01 | |
| (B) | tabletter
50 mg
(PharmaCoDane)
(kan dosisdisp.)
Captopril "Stada" |
023849 |
100 stk. (blister)
|
313,20 | 3,13 | 3,13 |
Foto og identifikation
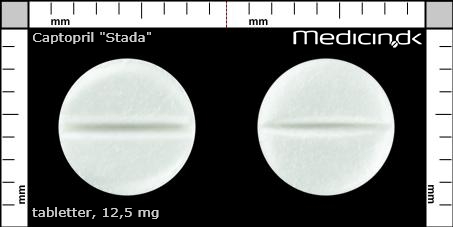
Tabletter 12,5 mg |
| Præg: |
Intet præg
|
| Kærv: | Delekærv |
| Farve: | Hvid |
| Mål i mm: | 6,1 x 6,1 |
Tabletter 25 mg |
| Præg: |
Intet præg
|
| Kærv: | Krydskærv |
| Farve: | Hvid |
| Mål i mm: | 8,1 x 8,1 |

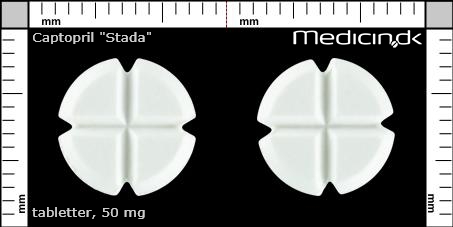
Tabletter 50 mg |
| Præg: |
Intet præg
|
| Kærv: | Krydskærv |
| Farve: | Hvid |
| Mål i mm: | 10,3 x 10,3 |
Referencer
3711. Janusinfo. Janusmed (Fosterpåverkan). Region Stochholm. 2021, https://janusmed.se/fosterpaverkan (Lokaliseret 18. marts 2026)
3878. Briggs GG, Freeman RK, Towers CV et al. Briggs: Drugs in Pregnancy and Lactation. Wolters Kluwer. 2021; 12th Edition, https://www.wolterskluwer.com/en/solutions/ovid/briggs-drugs-in-pregnancy-and-lactation-a-reference-guide-to-fetal-and-neonatal-risk-730 (Lokaliseret 19. marts 2026)
4331. Bateman BT, Patorno E, Desai RJ et al. Angiotensin-Converting Enzyme Inhibitors and the Risk of Congenital Malformations. Obstet Gynecol. 2017; 129(1):174-84, https://pubmed.ncbi.nlm.nih.gov/27926639/ (Lokaliseret 25. marts 2026)
4330. Polifka JE. Is there an embryopathy associated with first-trimester exposure to angiotensin-converting enzyme inhibitors and angiotensin receptor antagonists? A critical review of the evidence. Birth Defects Res A Clin Mol Teratol. 2012; 94(8):576-98, https://pubmed.ncbi.nlm.nih.gov/22807387/ (Lokaliseret 25. marts 2026)
4328. Li DK, Yang C, Andrade S et al. Maternal exposure to angiotensin converting enzyme inhibitors in the first trimester and risk of malformations in offspring: a retrospective cohort study. BMJ. 2011; 343, https://pubmed.ncbi.nlm.nih.gov/22010128/ (Lokaliseret 25. marts 2026)
4329. Walfisch A, Al-maawali A, Moretti ME et al. Teratogenicity of angiotensin converting enzyme inhibitors or receptor blockers. J Obstet Gynaecol. 2011; 31(6):465-72, https://pubmed.ncbi.nlm.nih.gov/21823839/ (Lokaliseret 25. marts 2026)
4327. Cooper WO, Hernandez-Diaz S, Arbogast PG. Major congenital malformations after first-trimester exposure to ACE inhibitors. N Engl J Med. 2006; 354(23):2443-51, https://pubmed.ncbi.nlm.nih.gov/16760444/ (Lokaliseret 25. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



