Yderligere information
|
Bemærk: Der er sket alvorlige fejl ved håndtering af dette lægemiddel. Typiske alvorlige fejl:
|
Direkte faktor Xa-hæmmer indeholdende rivaroxaban. DOAK (Direkte orale antikoagulantia).
Anvendelsesområder
Voksne
- Forebyggelse af venøs tromboemboli ved elektiv total hofte- eller knæalloplastik.
- Behandling af dyb venetrombose (DVT) og lungeemboli (LE) samt forebyggelse af recidiverende DVT og LE.
- I kombination med acetylsalicylsyre (ASA) eller med ASA og clopidogrel til forebyggelse af aterotrombotiske hændelser efter et akut koronarsyndrom (AKS) med forhøjede hjertemarkører.
- I kombination med ASA til forebyggelse af aterotrombotiske hændelser ved koronararteriesygdom (CAD) eller symptomatisk perifer arteriesygdom (PAD) med høj risiko for iskæmiske hændelser.
- Forebyggelse af apopleksi og systemisk emboli med øvrige tilfælde af atrieflimren/-flagren med en eller flere risikofaktorer, såsom:
- Apopleksi eller transitorisk iskæmisk attak i anamnesen
- alder ≥ 75 år
- hypertension
- diabetes
- hjerteinsufficiens.
Børn og unge < 18 årog legemsvægt ≥ 30 kg
- Behandling af venøs tromboemboli (VTE) og forebyggelse af recidiverende VTE.
Dispenseringsform
Tabletter. 1 tablet (filmovertrukken) indeholder 2,5 mg, 10 mg eller 15 mg rivaroxaban.
Doseringsforslag
Voksne
Knæalloplastik
- 10 mg dgl. i 14 dage.
- Første dosis 6-10 timer efter indgrebet.
Hoftealloplastik
- 10 mg dgl. i 35 dage.
- Første dosis 6-10 timer efter operation.
Forebyggelse af aterotrombotiske tilfælde efter AKS
- 2,5 mg 2 gange dgl. Fortsat behandling vurderes efter 12 mdr.
- Forsigtighed ved alder > 75 år og ved vægt < 60 kg.
- Forudgående apopleksi/TCI er kontraindicerende.
Forebyggelse af aterotrombotiske tilfælde ved CAD eller PAD
- 2,5 mg 2 gange dgl.
- Forsigtighed ved alder > 75 år og ved vægt < 60 kg.
- Patienter med tidligere hæmoragisk eller lakunær apopleksi, eller iskæmisk, ikke-lakunær apopleksi inden for den sidste måned er ikke undersøgt.
Behandling af DVT og lungeemboli samt forebyggelse af recidiverende DVT og lungeemboli
- Initialt 15 mg 2 gange dgl. i tre uger, derefter 20 mg 1 gang dgl. Individuel behandlingsvarighed.
- Ved GFR 15-49 ml/min: Initialt 15 mg 2 gange dgl. i tre uger, dernæst 15-20 mg dgl.
- Ved behandlingsvarighed > 6 mdr. 10 mg dgl. Ved høj tromboserisiko fastholdes 20 mg dgl. (GFR 15-49 ml/min. 15 mg dgl).
Forebyggelse af apopleksi og systemisk emboli
- 20 mg 1 gang dgl. Individuel behandlingsvarighed.
- Ved GFR 15-49 ml/min: 15 mg 1 gang dgl.
Beregn eGFR her: Beregning af eGFR ud fra CKD-EPI–formlen
Kardiovertering
Behandling med rivaroxaban kan initieres eller fortsættes hos patienter, der får behov for kardiovertering.
Børn og unge < 18 år og legemsvægt ≥ 30 kg
Behandling af VTE og forebyggelse af recidiverende VTE
- Behandling af VTE påbegyndes efter forudgående parenteral antikoagulansbehandling i mindst 5 dage.
- Legemsvægt 30-50 kg: 15 mg 1 gang dgl.
- Legemsvægt ≥ 50 kg: 20 mg 1 gang dgl.
- Børn med legemsvægt < 30 kg behandles kun med oral suspension.
- Behandlingen fortsættes i mindst 3 måneder og kan forlænges op til 12 måneder.
Bemærk
- Tabl. 15 mg skal indtages sammen med mad, da fødeindtagelse øger absorptionen fra ca. 66 % til ca. 90 %.
- Begrænset erfaring vedr. børn og unge < 9 år.
Skift fra anden oral AK-behandling til rivaroxaban
- Skift fra vitamin K-antagonist (VKA) til rivaroxaban
- Ved INR < 2,0 kan skift ske umiddelbart.
- Ved INR 2,0 - 2,5 kan skift ske dagen efter ophør med VKA, dvs. der holdes en dags pause.
- Skift fra andre DOAKs til rivaroxaban
- Seponér det fravalgte DOAK og start behandling med rivaroxaban på tidspunktet for næste dosis af oral antikoagulation.
Skift fra rivaroxaban til anden oral AK-behandling
- Skift fra rivaroxaban til vitamin K-antagonist (VKA)
- Ved skift fra rivaroxaban til VKA-behandling gives rivaroxaban og VKA initialt sideløbende.
- Børn skal fortsætte med rivaroxaban i 48 timer efter den første dosis af VKA.
- I de første to dage af skifteperioden gives standard-initialdosis af VKA, hvorefter VKA doseres ud fra INR-målinger.
- Blodprøve til INR-bestemmelse skal tages umiddelbart før næste dosis rivaroxaban, da rivaroxaban ellers vil bidrage til INR-stigningen.
- Rivaroxaban seponeres ved INR ≥ 2,0.
- Skift fra rivaroxaban til andet DOAK
- Seponér rivaroxaban og start behandling med det andet DOAK på tidspunktet for næste dosis af oral antikoagulation.
Skift mellem parenterale antikoagulantia og rivaroxaban
- Ved skift fra parenterale antikoagulantia til rivaroxaban påbegyndes rivaroxaban 0-2 timer før næste planlagte subkutane injektion af det parenterale antikoagulantia, som seponeres. Ved kontinuerlig intravenøs administration af parenteral antikoagulantia påbegyndes rivaroxaban på tidspunktet for seponering af det parenterale antikoagulante middel.
- Ved skift fra rivaroxaban til parenterale antikoagulantia skal første dosis af det parenterale antikoagulantia administreres på tidspunktet for næste planlagte administration af rivaroxaban, som seponeres.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-9 årBegrænset erfaring vedr. behandling af børn under 30 kg (ca. 9 år).
0-18 årErfaring savnes ved behandling af børn under 18 år. Sikkerhed og virkning er ikke klarlagt. Der foreligger begrænsede data.
Glemt medicin
- Dosis 2,5 mg x 2 dgl.: Der fortsættes med den regelmæssige dosis på næste skemalagte tidspunkt. Der må ikke tages dobbeltdosis som erstatning for manglende dosis.
- Dosis på 15 mg x 2 dgl.: Dosis tages straks (evt. begge doser) for at sikre en daglig dosis på 30 mg.
- Dosis 10 mg, 15 mg el. 20 mg x 1 dgl.: Dosis tages straks, og der fortsættes næste dag med dosis 1 x dgl. Der må ikke tages dobbeltdosis som erstatning for manglende dosis.
- Ved opkastning > 30 min. efter indtagelse skal dosis springes over, og næste dosis tages som planlagt.
Håndtering
| filmovertrukne tabletter 2,5 mg |
| filmovertrukne tabletter 10 mg |
Knusning/åbning
Kan knuses.
Administration
Knust tablet kan opslæmmes i vand.
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på kold, blød mad.
OBS
- Knust tablet kan opslæmmes i 50 ml vand og gives i en nasogastrisk sonde.
- Knuste tabletter er stabile i vand og æblemos i op til 4 timer.
| filmovertrukne tabletter 15 mg |
Knusning/åbning
Kan knuses.
Administration
Knust tablet kan opslæmmes i vand.
Mad og drikke
Tages med et glas vand.
Tages med mad.
Knust tablet kan kommes på kold, blød mad.
OBS
- Skal tages med mad pga. bedre optagelse.
- Knust tablet kan opslæmmes i 50 ml vand og gives i en nasogastrisk sonde.
- Knuste tabletter er stabile i vand og æblemos i op til 4 timer.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
forsigtighed, ingen eller begrænset erfaring |
|
|---|---|
| GFR | Advarsel |
| 15-30 ml/min. |
Ved GFR 15-30 ml/min. stiger plasmakoncentrationen af rivaroxaban signifikant. Bør derfor anvendes med forsigtighed. Børn: Bør ikke anvendes pga. manglende data. |
kontraindiceret, erfaring savnes |
|
|---|---|
| GFR | Advarsel |
| <15 ml/min. |
Bør ikke anvendes. |
Nedsat leverfunktion
Kontraindiceret ved leversygdom forbundet med koagulationsdefekt og klinisk relevant blødningsrisiko, herunder cirrosepatienter med Child-Pugh B-C.
Manglende erfaring vedr. børn og unge < 17 år.
Kontraindikationer
- Aktiv klinisk signifikant blødning
- Læsioner eller tilstande, hvor det anses som en signifikant risikofaktor for større blødninger, fx aktiv eller nylig gastrointestinal ulceration, tilstedeværelse af maligne tumorer med høj blødningsrisiko, nylig hjerne- eller rygskade, nylig hjerne-, ryg- eller øjenkirurgi, nylig intrakraniel blødning, kendte eller mistænkte esofagale varicer, arteriovenøse misdannelser, vaskulære aneurismer eller svære intraspinale eller intracerebrale vaskulære abnormaliteter.
- På grund af manglende undersøgelser frarådes behandling af patienter med mekaniske hjerteklapper.
- Samtidig behandling med andre antikoagulantia undtagen ved små doser heparin til opretholdelse af et åbent centralt vene- eller arteriekateter.
Forsigtighedsregler
- Øget blødningsrisiko, fx pga. ukontrolleret, svær arteriel hypertension.
- GFR 30-49 ml/min. og samtidig behandling med lægemidler, der kan øge koncentrationen af rivaroxaban, se interaktioner.
- Ved risiko for gastro-intestinal ulceration, bør profylakse overvejes.
- Spinal-/epiduralanæstesi eller spinalpunktur. Epiduralkateteret må først fjernes 18 timer (26 timer ved ældre) efter den seneste indtagelse af rivaroxaban, og næste dosis må tidligst gives 6 timer efter fjernelse. Hvis traumatisk punktur forekommer, skal indtagelse af rivaroxaban udskydes i 24 timer.
- DOAKs frarådes til patienter med tromboser i anamnesen, som er diagnosticeret med antifosfolipid-syndrom pga. mulig øget risiko for tilbagevendende trombotiske hændelser - sammenlignet med Vitamin-K-behandling. Dette gælder især højrisikogruppen, som er 3-dobbelt positive for lupus antikoagulans, anticardiolipin-antistoffer og anti-beta-2-glykoprotein-I-antistoffer.
Kirurgi og invasive indgreb
- Rivaroxaban seponeres før invasive indgreb eller kirurgi:
- GFR > 30 ml/min. Lav blødningsrisiko: mindst 24 timer før
- GFR > 30 ml/min. Høj blødningsrisiko: mindst 48 timer før
- GFR 15-29 ml/min. Lav blødningsrisiko: mindst 48 timer før
- GFR 15-29 ml/min. Høj blødningsrisiko: mindst 72 timer før
- Hvis indgrebet ikke kan udskydes, må den øgede blødningsrisiko afvejes mod behovet for hurtig intervention.
- Behandling med rivaroxaban bør genstartes hurtigst muligt efter indgreb, forudsat den kliniske situation tillader det, og adækvat hæmostase er opnået.
Typiske alvorlige fejl
| Beskrivelse | Konsekvens |
|---|---|
| Dobbeltordination. Man overså, at patienten i forvejen fik antitrombotisk behandling. | Død. |
| Fortsættelse af ordination uafhængigt af journalnotat og pausering i EPJ. | Blodtransfusion. |
| Manglende reordination/-administration af NOAK efter pausering. | Tromboemboli. |
| Overset forsigtighed/kontraindikation. Behandling gives på trods af, at patienten har øget risiko for blødning (under fx visse operationer og biopsier). | Blødninger. |
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Almindelige (1-10 %) | ||
| Blod og lymfesystem | Anæmi, Hæmoragisk diatese (Blødningstendens) | |
| Øjne | Okulær blødning | |
| Mave-tarm-kanalen | Abdominalsmerter, Gastro-intestinal blødning | Diarré, Dyspepsi, Gingival blødning, Kvalme, Obstipation, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Kraftesløshed, Pyreksi, Træthed | |
| Undersøgelser | Forhøjede levertransaminaser | Forhøjet carbamid i blodet, Forhøjet kreatinin i blodet |
| Knogler, led, muskler og bindevæv | Smerter i ekstremiteter | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Nyrer og urinveje | Hæmaturi, Nyrefunktionspåvirkning | |
| Det reproduktive system og mammae | Menoragi | |
| Luftveje, thorax og mediastinum | Hæmoptyse | Epistaxis |
| Hud og subkutane væv | Purpura | Hudkløe, Hududslæt |
| Vaskulære sygdomme | Hypotension, Hæmatom, Perifere ødemer | |
| Ikke almindelige (0,1-1 %) | ||
| Blod og lymfesystem | Trombocytopeni, Trombocytose | |
| Hjerte | Takykardi | |
| Mave-tarm-kanalen | Mundtørhed | |
| Almene symptomer og reaktioner på administrationsstedet | Utilpashed | |
| Lever og galdeveje | Leverpåvirkning | |
| Immunsystemet | Allergiske reaktioner, Angioødem | Urticaria |
| Undersøgelser | Forhøjet plasma-lipase og -amylase | |
| Hud og subkutane væv | Allergisk dermatitis | |
| Vaskulære sygdomme | Cerebral hæmoragi, Synkope | |
| Sjældne (0,01-0,1 %) | ||
| Lever og galdeveje | Hepatitis, Kolestase | Icterus |
| Undersøgelser | Forhøjet bilirubin | |
| Knogler, led, muskler og bindevæv | Muskelblødning | |
| Vaskulære sygdomme | Pseudoaneurisme | |
| Meget sjældne (< 0,01 %) | ||
| Immunsystemet | Anafylaktisk reaktion, Stevens-Johnsons syndrom | |
| Luftveje, thorax og mediastinum | Eosinofil pneumoni | |
| Hud og subkutane væv | Lægemiddelreaktion med eosinofili og systemiske symptomer - DRESS, Toksisk epidermal nekrolyse (TEN)* | |
Kliniske aspekter
*) Post marketing er set alvorlige hudreaktioner - som regel inden for de første to uger af behandlingen.
- Med ukendt frekvens er set nyresvigt og kompartmentsyndrom sekundært til blødning.
- Hos pædiatriske patienter blev hovedpine, feber, epistaxis og opkastning set meget almindeligt, og takykardi og forhøjet bilirubin almindeligt, hvilket er hyppigere end hos voksne.
Interaktioner
- Itraconazol, ketoconazol, voriconazol, posaconazol, HIV-proteasehæmmere og andre stærke hæmmere af både CYP3A4 og P-glykoprotein bør ikke anvendes, idet de øger plasmakoncentrationen af rivaroxaban med risiko for alvorlig blødning.
- Stærke og moderate hæmmere af CYP3A4, som hhv. clarithromycin og erythromycin, fluconazol, medfører stigning i AUC og Cmax, hvilket kan have betydning ved nedsat nyrefunktion.
- Rifampicin, phenytoin, carbamazepin, phenobarbital, naturlægemidler indeholdende perikon og andre stærke CYP3A4-induktorer kan nedsætte plasmakoncentrationen af rivaroxaban og bør undgås.
- Forsigtighed ved samtidig behandling med ASA og trombocythæmmende stoffer.
- Behandling med et NSAID må ikke igangsættes hos patienter, der er i behandling med et DOAK-præparat, medmindre dosisjustering er overvejet mhp. den øgede blødningsrisiko. Ved samtidig behandling med DOAK og NSAID skal patienten monitoreres for symptomer på blødninger og opfordres til straks at kontakte lægen ved mulige tegn på blødning.
- Samtidig behandling med andre antikoagulantia, undtagen i forbindelse med skift og ved små doser heparin til opretholdelse af et åbent centralt vene- eller arteriekateter, er kontraindiceret.
- Der kan være øget blødningsrisiko ved samtidig behandling med SSRI- og SNRI-præparater.
- Erfaring savnes med samtidig anvendelse af dronedaron, ticagrelor og prasugrel, som derfor bør undgås.
Graviditet
Baggrund: Der er data for < 200 gravide eksponeret i 1. trimester. Der er ikke tegn på væsentlig overhyppighed af medfødte misdannelser, men datamængden udelukker ikke en øget risiko. Risikoen for spontanabort synes øget, men dette kan også skyldes underliggende sygdom.
Se også: Klassifikation - graviditet
Amning
Bloddonor
Ingen karantæne ved tapning af plasma til fraktionering.
Doping

|
Ingen restriktioner |
Alkohol
Alkohol og Rivaroxaban Viatris påvirker ikke hinanden.
Følg dog altid Sundhedsstyrelsens anbefalinger om genstandsgrænser.
Forgiftning
Farmakodynamik
Farmakokinetik
- Biotilgængelighed 80-100 %.
- Metaboliseres overvejende i leveren.
- Ca. 33 % udskilles uomdannet gennem nyrerne.
- Plasmahalveringstid 5-9 timer (unge) og 11-13 timer (ældre).
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| filmovertrukne tabletter | 2,5 mg |
Farve
Andre
|
|
| 10 mg |
Farve
Andre
|
||
| 15 mg |
Farve
Andre
|
Firma
Tilskud
Tabletter 2,5 mg
- Klausuleret tilskud til patienter, som opfylder flg.:
- I tillæg til acetylsalicylsyre til:
- Patienter med symptomatisk perifer arteriesygdom i forlængelse af revaskularisering og høj tromboserisiko (samlet klinisk vurdering).
- Patienter med kronisk iskæmisk hjertesygdom, høj tromboserisiko (diabetes, tidligere akut myokardieinfarkt, perifer arteriesygdom) og lav/normal risiko for blødningskomplikation.
- For begge patientgrupper gælder, at i behandlingen skal være iværksat af en speciallæge i kardiologi eller karkirurgi.
- I tillæg til acetylsalicylsyre til:
En betingelse for at opnå tilskud er, at lægen har skrevet ”Tilskud” på recepten.
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | filmovertrukne tabletter
2,5 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
374870 |
56 stk. (blister)
|
72,30 | 1,29 | 10,33 | |
| (B) | filmovertrukne tabletter
2,5 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
549368 |
56 stk. (blister) (Orifarm)
|
Udgået 16-02-2026 | |||
| (B) | filmovertrukne tabletter
2,5 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
047586 |
100 stk. (blister)
|
50,75 | 0,51 | 4,06 | |
| (B) | filmovertrukne tabletter
2,5 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
061773 |
196 stk. (blister)
|
89,65 | 0,46 | 3,66 | |
| (B) | filmovertrukne tabletter
2,5 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
463673 |
196 stk. (blister) (Orifarm)
|
Udgået 13-04-2026 | |||
| (B) | filmovertrukne tabletter
10 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
401628 |
30 stk. (blister)
|
431,05 | 14,37 | 28,74 | |
| (B) | filmovertrukne tabletter
10 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
579290 |
100 stk. (blister)
|
883,00 | 8,83 | 17,66 | |
| (B) | filmovertrukne tabletter
15 mg
(kan dosisdisp.)
Rivaroxaban Viatris |
514397 |
42 stk. (blister)
|
54,20 | 1,29 | 1,72 |
Substitution
| filmovertrukne tabletter 2,5 mg |
|---|
| Rivaroxaban "Hexal" HEXAL, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaroxaban "Krka" KRKA, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaroxaban "Medical Valley" Medical Valley, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaroxaban "Orion" Orion Pharma, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaroxaban "Stada" STADA Nordic, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaroxaban "Zentiva" Zentiva, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaroxaban Accord Accord, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Rivaxa Glenmark Nordic, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| Xarelto Bayer, Rivaroxaban, filmovertrukne tabletter 2,5 mg |
| filmovertrukne tabletter 10 mg |
|---|
| Rivaroxaban "Krka" KRKA, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban "Medical Valley" Medical Valley, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban "Orion" Orion Pharma, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban "Sandoz" Sandoz, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban "Stada" STADA Nordic, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban "Teva" TEVA, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban "Zentiva" Zentiva, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Rivaroxaban Accord Accord, Rivaroxaban, filmovertrukne tabletter 10 mg |
| Xarelto Bayer, Rivaroxaban, filmovertrukne tabletter 10 mg |
| filmovertrukne tabletter 15 mg |
|---|
| Rivaroxaban "Krka" KRKA, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban "Medical Valley" Medical Valley, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban "Orion" Orion Pharma, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban "Sandoz" Sandoz, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban "Stada" STADA Nordic, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban "Stada" STADA Nordic, Rivaroxaban, hårde kapsler 15 mg |
| Rivaroxaban "Teva" TEVA, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban "Zentiva" Zentiva, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Rivaroxaban Accord Accord, Rivaroxaban, filmovertrukne tabletter 15 mg |
| Xarelto Bayer, Rivaroxaban, filmovertrukne tabletter 15 mg |
Foto og identifikation
Filmovertrukne tabletter 2,5 mg |
| Præg: |
RX, 1
|
| Kærv: | Ingen kærv |
| Farve: | Gul |
| Mål i mm: | 5,4 x 5,4 |

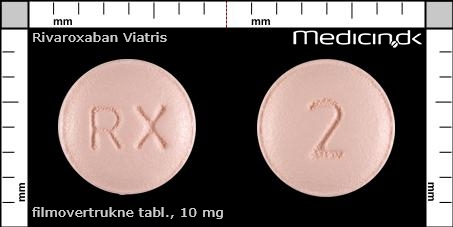
Filmovertrukne tabletter 10 mg |
| Præg: |
RX, 2
|
| Kærv: | Ingen kærv |
| Farve: | Lyserød |
| Mål i mm: | 5,5 x 5,5 |
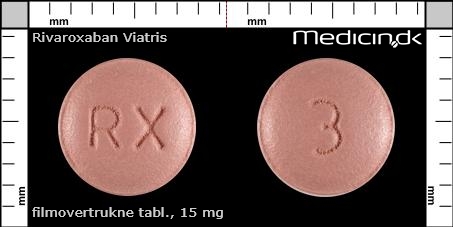
Filmovertrukne tabletter 15 mg |
| Præg: |
RX, 3
|
| Kærv: | Ingen kærv |
| Farve: | Rosa |
| Mål i mm: | 6,5 x 6,5 |
Referencer
4262. Lameijer H, Aalberts JJJ, van Veldhuisen DJ et al. Efficacy and safety of direct oral anticoagulants during pregnancy; a systematic literature review. Thromb Res. 2018; 169:123-7, https://pubmed.ncbi.nlm.nih.gov/30036784/ (Lokaliseret 25. marts 2026)
4261. Hoeltzenbein M, Beck E, Meixner K et al. Pregnancy outcome after exposure to the novel oral anticoagulant rivaroxaban in women at suspected risk for thromboembolic events: a case series from the German Embryotox Pharmacovigilance Centre. Clin Res Cardiol. 2016; 105:117-26, https://pubmed.ncbi.nlm.nih.gov/26195125/ (Lokaliseret 25. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



