Vil du vide mere?
Anvendelsesområder
- Hyperkolesterolæmi eller blandet dyslipidæmi, hvor diæt og andre livsstilsændringer ikke har haft tilstrækkelig effekt.
- Forebyggende til patienter med høj risiko for kardiovaskulære hændelser, som supplement til reduktion af andre risikofaktorer.
Dispenseringsform
Tabletter. 1 tablet indeholder 20 mg (delekærv) eller 40 mg (delekærv) pravastatinnatrium.
Doseringsforslag
Voksne
Individuelt efter behandlingsmål og respons.
- Initialt 10-40 mg som enkeltdosis sammen med aftensmåltidet.
- Sædvanlig vedligeholdelsesdosis 20-40 mg dgl.
- Maksimaldosis er 40 mg.
- Dosisjusteringer efter mindst 4 ugers behandling.
Børn 8-13 år
10-20 mg 1 gang dgl.
Unge 14-18 år
10-40 mg 1 gang dgl.
Bemærk:
- Behandling af børn og unge med heterozygot familiær hyperkolesterolæmi er en specialistopgave.
- Ingen erfaring vedr. børn < 8 år.
Børn og unge
-
Forsigtighed, ingen eller begrænset erfaring
0-8 årIngen erfaring. Børn får oftest målt kolesterol som led i udredning for familiær hyperkolesterolæmi. Målingen bør omfatte hele lipidprofilen, se Dyslipidæmi.
-
Forsigtighed, betinget
8-18 årBehandling af børn og unge med heterozygot familiær hyperkolesterolæmi er en specialistopgave. Børn får oftest målt kolesterol som led i udredning for familiær hyperkolesterolæmi. Målingen bør omfatte hele lipidprofilen, se Dyslipidæmi.
Håndtering
| tabletter 20 mg |
| tabletter 40 mg |
Knusning/åbning
Kan knuses.
Administration
Knust tablet kan opslæmmes i vand.
Mad og drikke
Tages med et glas vand.
Kan tages med eller uden mad.
Knust tablet kan kommes på en skefuld kold, blød mad, fx yoghurt eller æblemos.
Oplysningerne kan muligvis afvige fra produktresumé. Se endvidere Håndtering af tabletter og kapsler .
forsigtighed, dosisjustering |
||
|---|---|---|
| GFR | Alder | Advarsel |
| <30 ml/min. | 8-14 år |
Initialt 10 mg dgl. Kan øges til højst 20 mg dgl. |
| ≥14 år |
Initialt 10 mg dgl. Kan øges til højst 40 mg dgl. |
|
Nedsat leverfunktion
- Kontraindiceret ved aktiv leversygdom (Child-Pugh A, B og C) eller vedvarende alanin-aminotransferase (ALAT) forhøjelse > 3 gange øverste normalgrænse af ukendt årsag.
- Selv om leverpåvirkning forekommer sjældent, anbefales forsigtighed ved tidligere leversygdom, leverinsufficiens og stort alkoholforbrug.
- Initialdosis på 10 mg anbefales ved nedsat leverfunktion.
Kontraindikationer
Aktiv leversygdom eller vedvarende transaminaseforhøjelse over 3 gange øvre normalgrænse (UNL) af ukendt årsag.
Forsigtighedsregler
Risiko for hyperglykæmi
- Statiner kan øge blodsukkeret og medføre øget risiko for udvikling af diabetes - særligt ved disponering for type 2-diabetes.
- Type 2-diabetes disponerede patienter bør monitoreres nøje.
Risiko for udvikling af myopati og rhabdomyolyse
- Ved prædisponerende faktorer for rhabdomyolyse (fx ældre > 65 år, kvinder, nedsat nyrefunktion, ukontrolleret hypothyroidisme, alkoholmisbrug, arvelige muskulære sygdomme i familien) bør kreatinkinase måles før behandlingen. Hvis koncentrationen er mere end 5 gange øverste normalgrænse, bør målingen gentages efter 5-7 dage for bekræftelse. Er koncentrationen stadig forhøjet, bør behandlingen ikke startes.
- Ved uforklarede muskelsmerter, -svaghed, -ømhed eller -kramper, især hvis de ledsages af utilpashed eller feber, skal behandling pauseres og P-kreatinkinase måles.
- Overvej om p-kreatininkinase stigningen kan skyldes andet (fx fysisk aktivitet), tilstedeværelse af myopati, hvis P-kreatininkinasen forbliver høj, og hav in mente kombinationsterapi eller andet medikament som årsag (mulig interaktion).
- Hvis muskelsymptomerne forsvinder og P-kreatinkinasen normaliseres, kan behandlingen genoptages med lavest mulige dosis og under tæt monitorering.
Risiko for leverpåvirkning
- Selv om leverpåvirkning forekommer sjældent, anbefales forsigtighed ved tidligere leversygdom, leverinsufficiens og stort alkoholforbrug.
- ALAT bør måles ved symptomer, eller tilstedeværelsen af objektive fund tydende på leverpåvirkning.
- Dosisreduktion eller seponering ved ALAT over 3 gange øverste normalgrænse.
Bivirkninger
Registrerede bivirkninger |
||
| Systemorganklasse | Potentielt alvorlige bivirkninger | Oftest ikke alvorlige bivirkninger |
| Ikke almindelige (0,1-1 %) | ||
| Øjne | Synsforstyrrelser (herunder sløret syn og dobbelsyn) | |
| Mave-tarm-kanalen | Abdominalsmerter | Diarré, Dyspepsi, Flatulens, Gastro-øsofageal refluks, Kvalme, Obstipation, Opkastning |
| Almene symptomer og reaktioner på administrationsstedet | Træthed | |
| Immunsystemet | Urticaria | |
| Traumer, forgiftninger og behandlingskomplikationer | Senebetændelse (herunder seneruptur) | |
| Nervesystemet | Svimmelhed | Hovedpine |
| Psykiske forstyrrelser | Søvnforstyrrelser, Søvnløshed | |
| Nyrer og urinveje | Vandladningsbesvær (herunder dysuri, nykturi, ændret vandladningsfrekvens) | |
| Det reproduktive system og mammae | Seksuelle forstyrrelser | |
| Hud og subkutane væv | Alopeci | Hudkløe, Hududslæt |
| Sjældne (0,01-0,1 %) | ||
| Luftveje, thorax og mediastinum | Interstitiel lungesygdom | |
| Hud og subkutane væv | Fotosensibilitet | |
| Meget sjældne (< 0,01 %) | ||
| Mave-tarm-kanalen | Pancreatitis | |
| Lever og galdeveje | Fulminant levercellenekrose, Hepatitis | Icterus |
| Immunsystemet | Allergiske reaktioner, Anafylaktisk reaktion, Angioødem | |
| Knogler, led, muskler og bindevæv | Myopati, Myositis, Rhabdomyolyse (evt. med akut nyresvigt pga. myoglobinuri), Systemisk lupuslignende syndrom | |
| Nervesystemet | Paræstesier, Perifer neuropati* | |
| Hud og subkutane væv | Dermatomyositis | |
| Ikke kendt hyppighed | ||
| Lever og galdeveje | Fulminant leversvigt (herunder fatale tilfælde) | |
| Metabolisme og ernæring | Diabetes* (frekvens afhængig af eksisterende risikofaktorer) | |
| Knogler, led, muskler og bindevæv | Immunmedieret nekrotiserende myopati**, Muskelruptur | |
| Nervesystemet | Hukommelsesbesvær*, Myasthenia gravis, Okulær myasteni | |
| Psykiske forstyrrelser | Depression* | Mareridt* |
* Klasseeffekter set ved behandling med statiner.
** Persisterende muskelsvaghed og forhøjet P-kreatinkinase, der kan vedvare efter seponering.
Kliniske aspekter
- I enkelte tilfælde er set rhabdomyolyse, hos patienter i kraftig immunsuppressiv behandling med ciclosporin.
- Tilfælde af interstitiel lungesygdom er set særligt ved langtidsbehandling med statiner.
Interaktioner
- Øget risiko for muskelrelaterede bivirkninger (herunder rhadomyolyse) er set ved samtidig behandling med fibrater og statiner. Samtidig behandling med fibrater og pravastatin bør normalt undgås og hvis nødvendig kun foregå under nøje monitorering af kreatinkinase og kliniske tegn på muskelpåvirkning. Kombinationen er en specialistopgave.
- Samtidig indtagelse af anionbyttere reducerer biotilgængeligheden med 40-50 %, hvorfor statiner og anionbyttere skal indtages med mindst 4 timers interval.
- Ciclosporin, rifampicin og makrolider kan øge koncentrationen af pravastatin, og derved øges risikoen for myopati og rhabdomyolyse. Kombinationerne skal anvendes med forsigtighed. Der forventes ingen interaktioner mellem rifampicin og pravastatin, hvis de administreres med mindst 2 timers mellemrum.
- Ved samtidig anvendelse af fusidin og HMG-CoA-reduktasehæmmere som pravastatin øges risikoen for myopati. Pravastatin skal normalt midlertidigt seponeres ved behandling med fusidin - pravastatinbehandlingen kan genoptages 7 dage efter sidste dosis fusidin.
- Øget risiko for muskelbivirkninger er forekommet, når statiner kombineres med: Colchicin, nicotinsyre og lenalidomid. Forsigtighed anbefales.
- Pravastatin øger virkningen af vitamin K-antagonister. Monitorering af INR anbefales ved behandlingsstart, dosisjustering og seponering af pravastatin.
- Forsigtighed ved samtidig behandling med statiner og daptomycin pga. øget risiko for myopati. Pausering af statinbehandlingen bør overvejes under behandlingen med daptomycin.
Graviditet
Baggrund: Der er data for ca. 75 1. trimester-eksponerede uden tegn på overhyppighed af uønsket fosterpåvirkning. Datamængden tillader ikke at udelukke en øget risiko.
Se også: Klassifikation - graviditet
Amning
Bloddonor
Doping

|
Ingen restriktioner |
Alkohol
Forsigtighed ved indtag af alkohol under behandling med Pravastatinnatrium "Teva", da det kan give øget leverpåvirkning.
Ved kendt leversygdom og/eller indtag af store mængder alkohol i anamnesen, bør Pravastatinnatrium "Teva" bruges med forsigtighed.
Farmakodynamik
Selektiv hæmmer af hydroxymethylglutaryl-coenzym A (HMG-CoA)-reduktase, som er det hastighedsbestemmende enzym i kolesterolsyntesen. Øger dannelsen af LDL-receptorer, og bl.a. derved sænkes LDL-kolesterol i blodet.
Farmakokinetik
- Biotilgængelighed ca. 35 %.
- Maksimal plasmakoncentration efter ca. 1 time.
- Pravastatin er hydrofilt og passerer ikke blod-hjernebarrieren og optages sandsynligvis ikke i perifere celler. Derimod optages pravastatin ved aktiv transportmekanisme i levercellerne, hvor det således virker selektivt.
- Plasmahalveringstid ca. 1,5 timer.
- Udskilles hovedsageligt med galden.
Indholds- og hjælpestoffer
| Lægemiddelform | Styrke | Indholdsstoffer | Hjælpestoffer |
|---|---|---|---|
| tabletter | 20 mg |
Farve
Andre
|
|
| 40 mg |
Farve
Andre
|
Firma
Pakninger, priser, tilskud og udlevering
| Tilskud | Udlevering | Disp.form og styrke | Vnr. | Pakning | Pris | Pris enh. | Pris DDD. |
|---|---|---|---|---|---|---|---|
| (B) | tabletter
20 mg
(kan dosisdisp.)
Pravastatinnatrium "Teva" |
085651 |
100 stk. (blister)
|
48,90 | 0,49 | 0,73 | |
| (B) | tabletter
40 mg
(kan dosisdisp.)
Pravastatinnatrium "Teva" |
085669 |
100 stk. (blister)
|
Udgået 13-04-2026 |
Substitution
| tabletter 20 mg |
|---|
| Pravastatin "Sandoz" Sandoz, Pravastatin, tabletter 20 mg Genordn. B |
| Pravastatin "Stada" STADA Nordic, Pravastatin, filmovertrukne tabletter 20 mg Genordn. B |
| tabletter 40 mg |
|---|
| Pravastatin "Sandoz" Sandoz, Pravastatin, tabletter 40 mg Genordn. B |
| Pravastatin "Stada" STADA Nordic, Pravastatin, filmovertrukne tabletter 40 mg Genordn. B |
Foto og identifikation
Tabletter 20 mg |
| Præg: |
Intet præg
|
| Kærv: | Delekærv |
| Farve: | Lysegul |
| Mål i mm: | 8,7 x 8,7 |
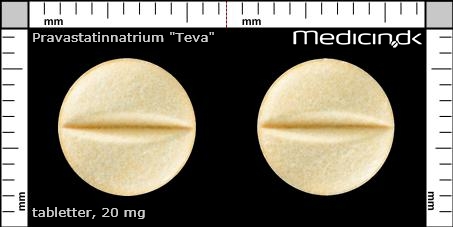
Tabletter 40 mg |
| Præg: |
Intet præg
|
| Kærv: | Delekærv |
| Farve: | Lysegrøn |
| Mål i mm: | 11,2 x 11,2 |
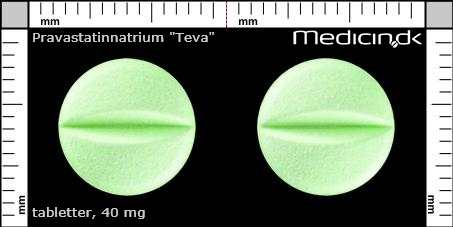
Referencer
6182. Karadas B, Uysal N, Erol H et al. Pregnancy outcomes following maternal exposure to statins: A systematic review and meta-analysis. Br J Clin Pharmacol. 2022; 88(9):3962-76, https://pubmed.ncbi.nlm.nih.gov/35639354/ (Lokaliseret 25. marts 2026)
4028. Bateman BT, Hernandez-Diaz S, Fischer MA et al. Statins and congenital malformations: cohort study. BMJ. 2015; 350, https://pubmed.ncbi.nlm.nih.gov/25784688/ (Lokaliseret 19. marts 2026)
Der kan forekomme forskelle mellem lægemiddelbeskrivelsen og indlægssedlen eller det myndighedsgodkendte produktresumé. Det skyldes, at Medicin.dk kan have suppleret Lægemiddelstyrelsens og medicinvirksomhedernes information med andre kilder. Lægemiddelbeskrivelsen og anden information i Medicin.dk’s produkter er til generel vejledning og kan ikke erstatte professionel medicinsk rådgivning.
Konsulter altid en læge eller anden sundhedsprofessionel ved spørgsmål om medicin, dosering eller behandling.
Læs mere om Brugervilkår og ansvar .



